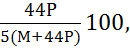|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Стабилизация эмульсий. Эмульгаторы
Строение Эмульсия – дисперсная система «жидкость - жидкость» (ж/ж). Для образования эмульсии обе жидкости должны быть нерастворимы или мало - растворимы друг в друге, а в системе должен присутствовать стабилизатор, называемый эмульгатором. Эмульсия тем седиментационно устойчивее, чем ближе плотность обоих фаз. Отличительной особенностью эмульсий является сферическая форма частиц (капель). Классификация эмульсий ü В зависимости от концентрации Wд дисперсной фазы различают эмульсии: · разбавленные (Wд<1%); · концентрированные (Wд<74%) ; · высококонцентрированные (Wд>74%). Системы газ/жидкость при малых концентрациях дисперсной фазы называются газовыми эмульсиями. Концентрированные системы газ/жидкость называются пенами. ü В зависимости от природы вещества ДФ и ДС различают: · эмульсии первого рода; · второго рода. Эмульсии первого рода или прямые эмульсии, состоящие из неполярной ДФ и полярной ДС, называются эмульсиями типа масло/вода (М/В). Эмульсии второго рода или обратные эмульсии, состоящие из полярной ДФ и неполярной ДС, называются эмульсиями типа вода/масло (В/М). При этом термин «вода» обозначает любую полярную жидкость, «масло» - неполярную. Маслом называют малополярные органические жидкости: бензол, бензин, керосин, анилин, минеральные и растительные масла, независимо от их химической природы. Например, дисперсия октана в этаноле – эмульсия типа М/В, дисперсия воды в октане – эмульсия типа В/М. Специфические свойства Для эмульсий характерным является свойство обращения фаз. При введении в эмульсию в условиях интенсивного перемешивания большого количества поверхностно-активных веществ (ПАВ), являющегося стабилизатором эмульсии противоположного типа, первоначальная эмульсия может обращаться, т.е. дисперсная фаза становится дисперсионной средой и наоборот (масло + вода = вода + масло). Все эмульсии термодинамически нестабильные структуры, за исключением критических эмульсий. Это структуры двух ограниченно растворимых жидкостей при температуре, близкой к критической. Методы получения Все методы получения эмульсий, как и любой другой дисперсной системы, можно разделить на конденсационные и диспергационные. Конденсационные методы связаны с образованием капелек эмульсии из отдельных молекул. Таким образом получаются критические эмульсии при выделении капель новой фазы из раствора вблизи критической температуры смешения. В промышленности и лабораторной практике эмульсии получают диспергированием одной жидкости в другой. В свою очередь, диспергационные методы можно разделить на методы, в основе которых лежит взбалтывание, и методы перемешивания. Диспергирование взбалтыванием производится при возвратно-поступательном движении либо сосуда, в котором находится смесь жидкостей, либо специального приспособления, например, спиральной пружины, находящейся внутри жидкости. Методы перемешивания основаны на использовании лопастных или пропеллерных мешалок. Иногда для приготовления эмульсии используют коллоидные мельницы. Общим для приготовления любой эмульсии является очередность смешения фаз. Всегда к жидкости, которая должна стать дисперсионной средой, постепенно прибавляется вторая жидкость. Для получения устойчивой эмульсии во внешней фазе уже должен присутствовать стабилизатор. Для облегчения диспергирования следует вводить эмульгатор, причем его можно растворять как в масляной, так и в водной фазе. 3.1 Устойчивость эмульсий. Наиболее частой ошибкой при получении эмульсий является неправильный выбор интенсивности механического воздействия. Часто считают, что эмульгирование происходит тем лучше, чем сильнее перемешивается (взбалтывается) смесь жидкостей. В действительности существует некоторая оптимальная интенсивность механического воздействия, выше которой происходит не диспергирование, а наоборот – коалесценция.В результате коалесценции эмульсия расслаивается на две непрерывные жидкие фазы. Коалесценция - самопроизвольный процесс, так как в результате слияния капелек эмульсии уменьшается площадь поверхности раздела фаз (∆Ω<0) и, соответственно, уменьшается энергия Гиббса системы (∆GΩ<0), (где∆Ω - приращение поверхности раздела фаз (м2). Аналогичный процесс коалесценции происходит в газовых эмульсиях при столкновении пузырьков газа. В результате коалесценции эмульсия перестает существовать как дисперсная система и полностью расслаивается на две непрерывные жидкие макрофазы: жидкость-жидкость или жидкость – газ. В жидкой дисперсной среде коалесценции часто предшествует коагуляция. Важный количественный метод определения устойчивости разбавленных и умеренно концентрированных эмульсий – изучение кинетики их коагуляции. Капли коалесцируют попарно, поэтому скорость коалесценции (коагуляции) Vкц описывается законом кинетики второго порядка, аналогичным уравнению кинетики быстрой коагуляции гидрофобных дисперсных систем : Vкц=kкц сv2 , Где сv - частичная концентрация эмульсии (число капель в единице объма, 1/л); kкц - константа скорости коалесценции. Стабилизация эмульсий. Эмульгаторы. Концентрированные двухкомпонентные эмульсии, приготовленные из полярной и неполярной жидкостей, неустойчивы и быстро расслаиваются. Устойчивые концентрированные эмульсии можно получить лишь в присутствии различных веществ – стабилизаторов, называемых эмульгаторами. Эмульгаторы – это вещества, образующие адсорбционный слой на поверхности раздела фаз дисперсная фаза (капли)/дисперсионная среда. Этот слой препятствует непосредственному соприкосновению капель и их слиянию (коалесценции). В качестве эмульгаторов могут применяться самые различные по природе вещества: поверхностно-активные вещества, молекулы которых содержат ионогенные полярные группы, (мыла в широком смысле слова), неионогенные поверхностно-активные вещества, высокомолекулярные соединения (ВМС). Эмульгирующей способностью обладают даже порошки. Стабилизация более или менее концентрированных эмульсий с помощью обычных неорганических электролитов невозможна вследствие недостаточной адсорбции их ионов на межфазной границе неполярный углеводород/вода. Стабилизация эмульсии с помощью поверхностно-активных веществ (ПАВ) обеспечивается благодаря адсорбции и определенной ориентации молекулы поверхностно-активного вещества (ПАВ), что вызывает понижение поверхностного натяжения. Кроме этого поверхностно-активные вещества (ПАВ) с длинными радикалами на поверхности капелек могут образовывать пленки значительной вязкости (структурно-механический фактор). Для эмульгаторов справедливо правило Ван - Крофта: эмульгаторы, растворимые в углеводороде, образуют эмульсии типа «вода в масле»; эмульгаторы, растворимые в воде, образуют эмульсии типа «масло в воде». Растворимость ПАВ характеризуется числом ГЛБ (гидрофильно-липофильный баланс). Чем оно больше, тем сильнее баланс сдвинут в сторону гидрофильных свойств, тем лучше данное вещество растворяется в воде. Для ГЛБ и неионогенных ПАВ Гриффин предложил эмпирические формулы. Для поликсиэтиленов и алкилфенолов формула имеет вид: ГЛБ = где 44 – молярная маса мономерной группы поликсиэтилена; Р – степень его полимеризации; М – молярная масса гидрофобного радикала. Уменьшение ГЛБ указывает на преобладание гидрофобных свойств молекул ПАВ. ПАВ с числом ГЛБ от 8 до 13 лучше растворимы в воде, чем в масле, и образуют эмульсии I рода. ПАВ с числом ГЛБ от 3 до 6 образуют эмульсии II рода. Для оценки эмульгаторов используют значения гидрофильного липофильного баланса (ГЛБ). В зависимости от числа гидрофильного липофильного баланса (ГЛБ) можно предположить тип образующейся эмульсии. Величина гидрофильного-липофильного баланса (ГЛБ) определяется разностью работ по адсорбции поверхностно-активных веществ (ПАВ) на границе раздела из одной и другой фаз. Значения гидрофильного-липофильного баланса (ГЛБ) даны в справочниках. 4. Методы разрушения. Эмульсии со временем разрушаются. В некоторых случаях возникает необходимость ускорить разрушение эмульсий, например, разрушение эмульсии в сырой нефти. Ускорить процесс разрушения можно всеми путями, ведущими к уменьшению прочности защитной пленки эмульгатора и увеличению возможности соприкосновения частиц друг с другом. Методов разрушения эмульсии (деэмульгирования) очень много. Наиболее важными из них являются следующие: ü химическое разрушение защитных пленок эмульгатора, например, действием сильной минеральной кислоты; ü прибавление эмульгатора, способного вызвать обращение фаз эмульсии и снижающего этим прочность защитной пленки; ü термическое разрушение - расслоение эмульсий нагреванием. С повышением температуры уменьшается адсорбция эмульгатора, что ведет к разрушению эмульсии; ü механическое воздействие. К этому методу относится механическое разрушение стабилизированных пленок, например, сбивание сливок в масло. Центрифугирование также относится к механическому воздействию; ü действие электролитов вызывает разрушение эмульсий, стабилизированных электрическим зарядом частиц; Часто стоит задача не получить эмульсию, а наоборот, предупредить ее возникновение или разрушить (деэмульгировать) уже образовавшуюся систему. Эмульсии типа м/в, полученные с применением ионогенных эмульгаторов, обычно разрушают с помощью коагуляции электролитами с поливалентными ионами. Так как такие электролиты, взаимодействуя с ионогенной группой эмульгатора, обычно дают соединения, нерастворимые, в воде, то введение их в систему равнозначно переводу эмульгатора в неактивную форму. Иногда для деэмульгирования эмульсий, полученных с применением ионогенных эмульгаторов, вводят в систему эмульгатор, способствующий образованию эмульсии обратного типа и таким образом как бы нейтрализующий действие первоначального эмульгатора. Следует заметить, что такой эмульгатор практически всегда образуется при введении электролитов с поливалентным катионом в эмульсии типа м/в, стабилизованные щелочными мылами, так как образующиеся при этом мыла с поливалентными катионами способствуют образованию эмульсий типа в/м. Эмульсии, стабилизованные неизношенными стабилизаторами разрушаются гораздо труднее. Электролиты разрушают такие эмульсии только при больших концентрациях, когда происходит уже не коагуляция, а высаливание. Более эффективным способом разрушения таких эмульсий является нагревание, вызывающее десорбцию молекул неионогенных стабилизаторов с капелек эмульсии или дегидратацию полярной части молекулы неионогенного-стабилизатора. Разрушение всех эмульсий можно достичь введением в систему поверхностно-активного вещества, вытесняющего из адсорбционного слоя эмульгатор, но неспособного стабилизовать эмульсию. При центрифугировании и фильтровании происходит собственно концентрирование эмульсии. Однако в эмульсиях с очень высокой концентрацией дисперсной фазы и недостаточным содержанием эмульгатора, как правило, происходит коалесценция капелек, и таким образом система разрушается. С. С. Воюцкий с сотрудниками разработал метод непрерывного разрушения эмульсий воды в углеводородах путем пропускания эмульсий через специальный фильтр. Капельки дисперсной фазы (воды) адсорбируются на фильтрующем материале, коалесцируют на его поверхности и стекают с фильтра (самоочищение фильтра). Разрушение эмульсий при повышении температуры обусловливается уходом эмульгатора с поверхности капелек в результате его десорбции или растворения в дисперсной фазе. Применение К природным эмульсиям относится ряд ценнейших растительных и животных продуктов. Так, эмульсией является молоко стабилизованная животными белками эмульсия жиров в воде. Молоко является сырьем молочной промышленности и служит для получения множества молочных продуктов - сливок, простокваши, кефира, масла, сыра и т; д. Природной эмульсией является также яичный желток. В пищевой промышленности к эмульсиям помимо молочных продуктов принадлежат такие продукты, как маргарин, майонез, различные соусы. В фармацевтической промышленности многие лекарства применяются в виде эмульсий, причем, как правило, для приема лекарств внутрь применяются, эмульсии первого рода, а эмульсии второго рода используются для наружного применения. Нефтяные эмульсии, деэмульгирование которых для освобождения от сильно засоленной воды является важнейшей задачей первичной переработки нефти. Близки к эмульсии кровь, а также системы, содержащие липосомы и микроорганизмы. В промышленности и технологии эмульсии используют в процессах эмульсионной полимеризации, в качестве смазочно-охлаждающих жидкостей, в виде заменителей цельного молока, как смазки, составы для консервации, проклеивающие составы в производстве бумаги, аппретуры для улучшения свойств и прокрашивания кожи, препараты для обработки нитей и тканей. Обратные эмульсии служат буровыми растворами при проходке нефтяных и газовых скважин, для обработки призабойных зон в них; перспективно использование микроэмульсий для увеличения степени нефтеотдачи пластов. Разнообразные обратные эмульсии применяются в виде лекарств и косметических мазей и кремов, пищевых продуктов (напр., маргарин). Прямые эмульсии перфторуглеродных соед. в воде -перспективные кровезаменители. Также применяют процессы акустического эмульгирования (а часто и сопутствующие им по условиям технологии последующие процессы деэмульгирования) перспективно использовать при мыловарении, при обезвоживании сырой нефти и очистке нефтяных емкостей и танкеров, в технологии производства пищевых продуктов (сливочного масла, маргарина), при получении битумных (асфальтовых) эмульсий, при переработке эмульсий натурального каучука, получения консистентных смазок, охлаждающих жидкостей для металлообработки, при производстве эмульсионных красок (водо-дисперсионных, водоэмульсионных и латексных) и т.д. В обязательном ассортименте лекарственных средств, выпускаемых по методам как заводской, так и аптечной технологии, значительное место занимают лекарственные эмульсии. К ним, например, относятся альбихоловая и нафталановая эмульсии, масляные эмульсии, противоожоговые эмульсии. Действующие субстанции в эмульгированной форму лучше усваиваются, оказывают меньшее раздражающее действие на слизистую оболочку, более точно дозируется. В фармацевтической практике под эмульсиями, как лекарственными формами, понимают только дисперсные системы типа М/В для внутреннего употребления(серебра протеинат, колларгол, эмульсии касторового масла, парафина жидкого (вазелиновое масло)). Однако эмульсионное состояние достаточно часто встречается в других лекарственных формах – мазях, линиментах, суппозиториях, пилюлях (синтомицина линименты, алоэ древовидного листья, тезана и т.д.), представляющих собой дисперсные системы обоих типов (чаще всего это обратные эмульсии). Прямые эмульсии В/М и при приеме внутрь действуют по-разному: эмульсии В/М быстро смешиваются с пищеварительными соками и обычно легко усваиваются организмом. Обратные эмульсии М/В ведут себя аналогично жирам. Как правило, обратные эмульсии при приеме внутрь действуют слабее, так как для их равномерного распределения в пищеварительных соках требуются дополнительное эмульгирование и длительное время. При наружном применении (нанесении на кожу) действующие субстанции из эмульсий типа В/М легче проникают через эпидермис и в более глубокие ткани. Эмульсии же типа «масло-вода», подобно большинству водных жидкостей, плохо смачивает кожу, и действующие субстанции менее биодоступны.
Список литературы: 1. Коллоидная химия. Физическая химия дисперсных систем : учеб. для студентов учреждений высш. проф. образования, обучающихся по специальности 060301.65 "Фармация" по дисциплине "Физ. и коллоид. химия" / Ю. А. Ершов. - М. : ГЭОТАР-Медиа, 2012. - 352 с. 2. Физическая и коллоидная химия : учебник / Под ред. проф. А.П. Беляева. - М. : ГЭОТАР-Медиа, 2010. - 704 с. 3. А.И. Болдырев. Физическая и коллоидная химия. Москва. «Высшая школа». 1974г. - 504с. 4. Д.А. Фридрихсберг. Курс коллоидной химии. Ленинград. «Химия». 1984г. - 386с. 5. www.Xumuk.ru
Поиск по сайту: |