 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Задачи по курсу «Катализ»
1. Присутствие катализатора позволяет уменьшить энергию активации с 50 до 30 кДж. а) Во сколько раз увеличится скорость каталитической реакции по сравнению с некаталитической, при условии, что все другие факторы скорости реакции остаются неизменными. б) При какой температуре каталитическая реакция протекала бы с такой же скоростью, что и некаталитическая при 5000С. Какие преимущества дает использование катализатора.
2. Составить уравнение себестоимости продукта В, получаемого согласно уравнению А ® В и получить ее значение в каталитическом и некаталитическом вариантах, если в первом случае степень превращения реагента А равна хА=0,9, стоимость 1 кг катализатора составляет 2000 руб., а его расход на 1 т продукта В 0,5 кг/т, амортизационные отчисления соответствуют 0,15 в год от стоимости оборудования реакционного узла, которая составляет 4000000 руб. При этом стоимость рецикла в расчете на 1 т продукта В равна 5000 руб./т, стоимость сырья (А) – 3000 руб./т, перечисляемая зарплата – 1920000 руб. в год, годовая производительность – 40000 т. Во втором случае хА=0,7, норма амортизационных отчислений – 0,05, стоимость рецикла, сырья и годовая зарплата – те же.
3. Каталитическая реакция А ® В осуществляется с безвозвратной потерей непрореагировавшего А. Составить уравнение себестоимости для каталитического и некаталитического вариантов процесса и найдите ее значение, исходя из условий в задаче 2.
4. Найдите оптимальный профиль температуры для производительности обратимой экзотермической реакции
если константы скорости прямой и обратной реакций составляют соответственно
5. Выведите кинетическое уравнение для реакции конденсации нитрометана с ацетоном
если известно, что скорость лимитируется стадией атаки молекулы кетона карбанионом нитросоединения, образующимся под действием щелочи, по обратимой реакции, константа равновесия которой достаточно велика.
6. Каков механизм реакции А ® В + Z на поверхности катализатора при следующих кинетических уравнениях а) б) В каких из приведенных случаев будет наблюдаться экстремальная зависимость скорости реакции от давления?
7. Гетерогенно-каталитическая реакция А + Y ® B протекает в кинетической области и описывается уравнением скорости
Найдите аналитическое решение для максимума начальной скорости процесса в зависимости от мольного соотношения исходных реагентов, если процесс проводится при постоянном общем давлении Р0 в отсутствие посторонних разбавителей. Какой вывод следует из этого для реакции гидрирования ненасыщенных соединений, адсорбционный коэффициент которых больше, чем у водорода.
8. Скорость автокаталитической реакции Решите это кинетическое уравнение и найдите выражение степени превращения от времени реакции, если [A]0=а, [P]0= р.
9. Нарисуйте графики зависимости концентрации веществ А и В от времени в обратимой реакции А а) k1 > k–1 б) k1 < k–1 . В обоих случаях начальная концентрация В не равна 0.
10. Получены данные по зависимости начальной скорости реакции от рН среды
Рассчитайте значения параметров
11. Эффективная константа скорости некоторой кислотно-основно-каталитической реакции выражается зависимостью kэф. = k0 + Нарисуйте графическую зависимость скорости реакции от рН среды.
12. В системе протекают две параллельные реакции, основная
и побочная
С ростом температуры доля побочного продукта С возрастает. какая причина лежит в основе этого явления? а) Е1 > E2; б) Е1 < E2; в) А1 > А2; г) А1 < А2
13. Как будет меняться соотношение продуктов параллельных реакций
с увеличением степени превращения реагента А? а) увеличится; б) уменьшится; в) останется неизменным
Поиск по сайту: |

 A
A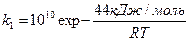 и
и  .
. в) r = k ∙ PA
в) r = k ∙ PA г)
г) 
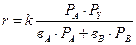
 описывается кинетическим уравнением r = k[A][P].
описывается кинетическим уравнением r = k[A][P]. В для следующих случаев
В для следующих случаев ,
,  , k0 .
, k0 .


