 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Электролиз. Различные виды электролиза и применение их на практике. Катодные и анодные процессы. Нанесение металлических покрытий. Законы электролиза ⇐ ПредыдущаяСтр 2 из 2
Электролизом называют процессы, происходящие на электродах под действием электрического тока, подаваемого от внешнего источника. При электролизе происходит превращение электрической энергии в химическую. Электрод, на котором идет реакция восстановления (катод), у электролизера подключен к отрицательному полюсу внешнего источника тока. Электрод, на котором протекает реакция окисления (анод ), подключен к положительному полюсу источника тока. Электролиз широко применяется в современной промышленности. Он является одним из способов промышленного получения алюминия, водорода, а также гидроксида натрия, хлора, хлорорганических соединений, диоксида марганца[2], пероксида водорода. Большое количество металлов извлекаются из руд и подвергаются переработке с помощью электролиза (электроэкстракция, электрорафинирование). Электролиз находит применение в очистке сточных вод (процессы электрокоагуляции, электроэкстракции, электрофлотации). Катодные процессы. При прочих равных условиях ионы металлов восстанавливаются на катоде тем легче, чем менее активен металл, чем дальше вправо он расположен в ряду напряжений. 1) Катионы металлов, имеющие электродный потенциал более высокий, чем у ионов водорода Н+ (в ряду напряжений эти металлы стоят после Н2), при электролизе практически полностью восстанавливаются на катоде: Cu2+ + 2e → Cu0 2) Катионы металлов, имеющие низкую величину электродного потенциала (от начала ряда напряжения по алюминий включительно), не восстанавливаются на катоде и остаются в растворе, на катоде идет процесс электрохимического восстановления водорода из молекул воды: 2H2O + 2e → H2 + 2OH¯ 3) Катионы металлов, имеющие электродный потенциал ниже , чем у ионов водорода (Н+), но выше, чем у ионов алюминия (Al3+), т.е стоящих между Zn2+→ Men+ ← H2, при электролизе восстанавливаются на катоде одновременно с водородом. Fe3+ + 3e → Fe0 2H2O + 2e → H2 + 2OH¯ Таким образом, характер катодного процесса при электролизе водных растворов электролитов определяется, прежде всего, положением соответствующего металла в ряду напряжения. Анодные процессы. При электролизе веществ используется инертные, не изменяющиеся в процессе электролиза аноды (графитовые, платиновые) и растворимые аноды, окисляющиеся в процессе электролиза легче, чем анионы (из цинка, никеля, серебра, меди и других металлов). 1) Анионы бескислородных кислот (S2ˉ, I¯, Br¯, Cl¯) при их достаточной концентрации легко окисляются до соответствующих простых веществ. 2) При электролизе водных растворов щелочей, кислородсодержащих кислот и их солей, а также плавиковой кислоты и фторидов происходит электрохимическое окисление воды с выделение кислорода: в щелочных растворах: 4OH¯ - 4e → O2 + 2H2O в кислых и нейтральных растворах: 2H2O - 4e → O2 + 4H+ Для нанесения на поверхность тонкого металлического слоя — гальванического покрытия — применяется электролиз. Перед покрытием изделия необходимо тщательно очистить, иначе металл будет осаждаться неравномерно, и связь металла с поверхностью изделия будет неустойчивым. С помощью электролиза можно покрыть деталь тонким слоем золота или серебра, хрома или никеля. С помощью электролиза можно наносить тончайшие металлические покрытия на различные металлические поверхности. При таком способе нанесения покрытий, деталь используют как катод, содержащийся в раствора соли того металла, покрытие из которого необходимо получить. В качестве анода используется пластинка из того же металла. Количественные характеристики электролиза выражаются двумя законами Фарадея: 1) Масса вещества, выделяющегося на электроде *, прямо пропорциональна количеству электричества, прошедшего через электролит *. 2) При электролизе различных химических соединений одинаковые количества электричества выделяют на электродах массы веществ, пропорциональные их электрохимическим эквивалентам. Эти два закона можно объединить в одном уравнении: где m – масса выделяющегося вещества, г; n – количество электронов, переносимых в электродном процессе; F – число Фарадея (F=96485 Кл/моль) I – сила тока, А; t – время, с; M – молярная масса выделяющегося вещества, г/моль. Величина
Поиск по сайту: |
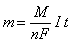 ,
, называется электрохимическим эквивалентом вещества.
называется электрохимическим эквивалентом вещества.