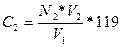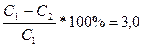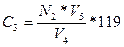|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Экспериментальная часть. Объёмный феррофосфатно-ванадатный метод определения урана.
Объёмный феррофосфатно-ванадатный метод определения урана. Объемные методы основаны на реакции О-В или комплексообразования. Цель работы: освоение теории и практики объёмного феррофосфатно-ванадатного метода определения урана. Экспрессный феррофосфатно-ванадатный метод определения урана разработан В.С., Сырокомским в 1959 году и основан на восстановление урана (VI) до урана(IV) с последующим титрованием урана(IV) раствором ванадата аммония. Механизм процесса определения урана (VI) складывается из следующих стадий: 1. Быстрое (в течение 5 минут) и полное восстановление уранил-иона выпоняют с применением соли Мора в присутствии значительного избытка фосфорной кислоты в соответствие с реакцией: UO2SO4 + 2FeSO4 + 7H3PO4 = H2[U(IV)(HPO4)3] + 2H[Fe(III)(HPO4)2] + 3H2SO4 + 2H2O Фосфатные комплексы урана(IV) и железа(III) отличаются более высокой устойчивостью по сравнению с фосфатными комплексами уранил-иона и иона железа(II), это приводит к увеличению скорости восстановления и способствует смещению равновесия реакции вправо. 2. Избыток железа(II) окисляют концентрированной азотной кислотой: FeSO4 + HNO3 + 2H3PO4 = H[Fe(HPO4)2] + NO2 +H2SO4 + H2O Реакция окисления железа(II) происходит с образованием других оксидов азота. При введении азотной кислоты тонкой струей появляется коричневая окраска иона железа(II), которая исчезает вследствие образования бесцветного фосфатного комплекса. Для полного окисления железа(III) необходим избыток азотной кислоты. Урана (IV), присутствующий в виде прочного фосфатного комплекса, не окисляется азотной кислотой. Сопутствующие урану примеси – ионы молибдена, мышьяка и некоторых других элементов окисляются азотной кислотой до высших степеней окисления и не мешают определению урана. Избыточная азотная кислота связывается введением раствора мочевины 3. Титрование урана(IV) раствором ванадата аммония происходит в соответствии со следующей суммарной реакцией: U4+ + 2VO3- +4H+ = UO22+ + 2H2O+2VO2- H2[U(IV)(HPO4)3]+ 2NH4VO3 + 2H2SO4 = UO2SO4 + 2H2O+2VO2- Ионы урана(IV) до урана(VI) ионами ванадия(V) окисляются очень быстро, это делает возможным прямое титрование урана(IV) даже разбавленными растворами солей ванадия (0,01-0,001М). Ход работы: Реактивы и оборудование.
Экспериментальная часть Отобрать две пробы по 5 см3 раствора с концентрацией урана 1 - 2 г/л.
Таблица «Условия и результаты определения урана объёмным методом»
Вывод: В ходе работы было определено содержание урана в анализируемом растворе, объёмным феррофосфатно-ванадатным методом, составившее 60 мг.
Поиск по сайту: |