 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Теоретичні основи визначення кількісного вмісту катіонів в розчинах води на основі електролізу
Струм–це впорядкований рух електронів. Якщо ми візьмемо атом в якому є ядро навколо якого навколо якого по орбіталях будуть рухатись електрони. Саме ж ядро складається з двох елементарних частинок: протонів і нейтронів . Де протони несуть позитивний потенціал ядра, а електрони несучи негативний потенціал створюють електричний баланс в атомі. Якщо ми перейдемо до струму, то це означає, що у нас є замкнуте коло і є різниця потенціалів. Відповідно взявши одну частину води і встановивши її вище (тобто створити позитивний потенціал), а іншу частину води поставити нижче (створивши негативний потенціал), дати можливість води до вільного протікання, то вода потече з вищого місця в нижче, це саме й відбувається і в електронних колах, тільки коли коло замкнене і є можливість вільного руху електронів, цей рух відбувається. Даний рух і є – електричним струмом. Протікання струму можливе лише в металах, це пов’язано з будовою металів, зазвичай це останній електрон не дуже сильно прив’язаний до ядра і він може не перебувати на своїй орбіті , а десь бути поза межами. Таким чином у металів, у яких є багато таких атомів, які поєднані металевими кристалічними гратками можуть вільно блукати від одного атома до іншого мігруючи електрони. Відповідно як тільки з’являється цей потенціал додатковий, зовнішні ці електрони відразу починають рухатись не хаотично, а впорядковано у даному напрямку по провіднику. Такий же самий принцип протікання електронів і по електролітах. Електроліти – це речовини, а саме може бути і вода, в якій певна кількість дисоційованих частинок, які можуть переносити вільні електрони. Ідеальний електроліт – це той електроліт який дисоціює наявність на йони. Якщо ми візьмемо будь-яку речовину і про дисоціюємо у воді, то розпад на йони може відбуватись частково, тобто частини молекул розпадаються на йони, а частково ні. Ті молекули, які не про дисоціювали, вони в процесі проходження через різні речовини або осаджуються або вступають у реакцію і відповідно іншим чином виявляються. Тобто залишаються тільки ті, які є дисоційованими і можуть вільно рухатись разом з водою. Коли ж йони розчиняються у воді також починають рухатись і по всій (товщі) території води, тому що вода має чітку обмежену кристалічну гратку. Відповідно всі молекули в рідинах хаотично рухаються і не можуть покидати межі речовини в якій вони знаходяться. Якщо ми візьмемо, наприклад, декілька йонів, які розміщуються один біля одного, то коли створюється зовнішній енергетичний потенціал на пластинці вони можуть передавати цей електрон. При цьому , що цікаво крім того, що вони можуть передавати цей електрон, створюється напруга під час удару йон проходить вздовж лінії напруження. Якщо є електричне поле то цей струм створює електричне поле і називається напруженістю електричного поля, що є векторною величиною, яка задає напрям руху. Відповідно до напряму руху, напруженість електричного поля, тобто дані електрони можуть задавати рух і створювати правило йонів. Тобто таким чином у нас є два види руху: електричний (той рух , який передається електроном); рух самих йонів. Якщо взяти до уваги ці два фактори, про те що електроліт може передавати електрони і безпосередньо створювати впорядкований рух самих йонів, то ми за допомогою цих двох факторів можемо визначити точно, які у нас йони, та яка їх кількість і спробувати розписати повністю склад даного електроліту. Тому кожен йон має свою певну масу і відповідно до цього він має свою власну швидкість переміщення в речовині, також він має досить цікавий процес, під час свого руху в нього частково змінюється його зовнішня орбіталь в протилежному напрямку. Наприклад, якщо ми розглянемо I групу, то діаметр гідратованої молекули і сам радіус буде зменшуватись, а вага збільшуватиметься. Наприклад рух гідратованого цезію буде швидший, а ніж рух гідратованого літію. Оця цікава функція, що є в природі і пов’язана з електролітами дасть нам можливість визначити точну кількість, яка передається змінюючи напругу і виконувати різні розрахунки. Для проведення відповідних розрахунків ми скористаємось двома законами Ома і Фарадея. Закон Ома стверджував, що є пропорційність сили струму у провіднику до прикладеної напруги. На основі закону Ома ми зможемо визначити кількісний склад йонів, тобто ми знайдемо N для всіх йонів скільки там є , відповідно ми зможемо знайти точну масу всієї речовини, але ще потрібно врахувати то що в розчині можуть бути і інші сполуки. Тому Закон Ома справедливий для провідників, виготовлених із матеріалів, у яких є вільні носії заряду: електрони провідності, дірки або іони Якщо до таких провідників прикласти напругу, то в провідниках виникає електричне поле, що змушуватиме носії заряду рухатися. В середньому носії заряду мають швидкість, яка визначається частотою зіткнень. Математичною характеристикою таких зіткнень є час розсіяння і зв'язана із ним довжина вільного пробігу носіїв заряду. Обчислення показують, що середня швидкість носіїв заряду пропорційна прикладеному електричному полю, а отже й напрузі. Таким чином, у матеріалах із вільними носіями заряду сила струму пропорційна напруженості електричного поля. У сильних електричних полях закон Ома часто не виконується навіть для гарних провідників, оскільки фізична картина розсіяння носіїв заряду змінюється. Розігнаний до великої швидкості носій заряду може іонізувати нейтральний атом, породжуючи нові носії заряду, які теж у свою чергу вносять вклад у електричний струм. Електричний струм різко, іноді лавиноподібно, наростає. В електротехніці прийнято записувати закон Ома і інтегральному вигляді де U — прикладена напруга, I — сила струму, R — електричний опір провідника. Проте опір є характеристикою провідника, а не матеріалу, й залежить від довжини та поперечного перерізу провідника. Тому в фізиці застосовують закон Ома у диференціальному вигляді:
де j — густина струму, σ — питома провідність матеріалу, E — напруженість електричного поля. Питома провідність залежить від кількості вільних носіїв заряду в провіднику і від їхньої рухливості. Еквівалентність двох форм запису Різниця потенціалів (напруга) на кінцях провідника довжиною
Закóн Фарадéя – основні закони електролізу. Встановлюють взаємозв’язок між кількістю електрики, яка проходить через електропровідний розчин (електроліт), і кількістю речовини, яка виділяється на електродах. Перший закон: маса m речовини, яка виділилась на електроді під час проходження електричного струму, прямо пропорційна значенню q електричного заряду, пропущеного крізь електроліт,
де k – електрохімічний еквівалент речовини, m - маса речовини, q - заряд . Другий закон: електрохімічні еквіваленти елементів прямо пропорційні їх хімічним еквівалентам.
де A - атомна маса речовини, Користуючись цими законами ми точно можемо знайти яка є маса і кількість цих іонів, відповідно масова доля і дійти до якісного й кількісного складу використовуючи один електролізер.
Поиск по сайту: |


 з постійною напруженістю електричного поля
з постійною напруженістю електричного поля 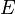 дорівнює
дорівнює
 ,
,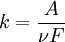 ,
, - заряд її йона, F - число Фарадея. Частка A/ν називається хімічним еквівалентом.
- заряд її йона, F - число Фарадея. Частка A/ν називається хімічним еквівалентом.