 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Классификация вторичных энергетических ресурсов промышленности
ВЭР промышленности делятся на три основные группы: – горючие,– тепловые,– избыточного давления. Горючие (топливные) ВЭР – химическая энергия отходов технологических процессов химической и термохимической переработки сырья, а именно это: – побочные горючие газы плавильных печей (доменный газ, колошниковый, шахтных печей и вагранок, конверторный и т.д.), – горючие отходы процессов химической и термохимической переработки углеродистого сырья (синтез, отходы электродного производства, горючие газы при получении исходного сырья для пластмасс, каучука и т.д.), – твёрдые и жидкие топливные отходы, не используемые (не пригодные) для дальнейшего технологической переработки, – отходы деревообработки, щелока целлюлозно-бумажного производства. Горючие ВЭР используются в основном как топливо и немного (5%) на не топливные нужды (преимущественно в качестве сырья).Тепловые ВЭР – это тепло отходящих газов при сжигании топлива, тепло воды или воздуха, использованных для охлаждения технологических агрегатов и установок, теплоотходов производства, например, горячих металлургических шлаков.
«Аналитическая химия» 1. Ионная сила раствора. Активность. Коэффициент активности. Влияние заряда иона на величину коэффициента активности. Электролиты, практически полностью диссоциирующие в водных растворах, называются сильными электролитами. К сильным электролитам относятся:(HCl, HBr, HI, HClO4, HNO3).В растворах сильных электролитов вследствие их полной диссоциации велика концентрация ионов. Свойства таких растворов существенно зависят от степени взаимодействия входящих в их состав ионов как друг с другом, так и с полярными молекулами растворителя. В результате свойства раствора, зависящие от числа растворенных частиц, такие, как электропроводность, понижение температуры замерзания, повышение температуры кипения и т. д., оказываются слабее, чем следовало бы ожидать при полной диссоциации электролита на невзаимодействующие ионы. Поэтому для описания состояния ионов в растворе наряду с концентрацией ионов пользуются их активностью, т. е. эффективной(активной) концентрацией, с которой они действуют в химических процессах. Активностью иона называется эффективную или условную концентрацию в соответствии которой он действует в химич.реакциях.аА= fА *[A],где fА – коэффициент активности,отражающий отклонение реальной системы от идеальной.Коэффициенты активности меняются в широких пределах. В разбавленных растворах их значения зависят в основном от концентрации и заряда ионов, присутствующих в растворе, т. е. от "ионной силы"раствора I, которая равна: I=1/2* ∑ CiZi2 .Расчет коэффициента активности по теории Дебая-Хюккеля:еслиI<0,01 ,то –lgfi=0,5*zi2*√I.Пример:I=0,01 -lgfNa+=0,5*12*√0,01=0,05. fNa+=10-0,05=0,89. ai=fi*[Ci],ai=0,0089моль/л.Если 0,01<I<0,1, -lgfi=0,5*zi2*√I/1+√I.Если I>0,1. –lgfi=[0,5*zi2*√I/1+√I]-0,1*Z2*I.(Ур-еДевиса)
2. Кислоты и основания по теории Бренстеда-Лоури. Константы кислотности и основности сопряженных пар. Протолитическая (протонная) теория кислот и оснований была предложена в 1923 году независимо друг от друга датским учёным Й. Брёнстедом и английским учёным Т. Лаури. В ней понятие о кислотах и основаниях было объединено в единое целое, проявляющееся в кислотно-основном взаимодействии: А
Аналогично для протолиза слабого основания NH3·HOH ↔ NH4+ + OH–существует константа основности:
3. Явление автопротолиза. Ионное произведение воды. Водородный показатель. Гидроксильный показатель.
Чистая вода обладает незначительной электрической проводимостью, которая объясняется небольшой диссоциацией воды на ионы водорода и гидроксид-ионы: H2O Такой процесс называется автопротолизом (самодиссоциацией). По величине электропроводности чистой воды можно вычислить концентрации ионов H+ и OH–. При 25°С они равны по 10–7 моль/л. Выражение для константы диссоциации * воды имеет вид: По признаку влияния на относительную силу электролитов и по способности изменять соотношение в силе электролитов различают дифференцирующие и нивелирующие растворители. К нивелирующим относят растворители, в среде которых уравнивается сила кислот, оснований или солей, к дифференцирующим — растворители, в среде которых проявляются значительные различия в силе электролитов. В зависимости от ряда факторов один и тот же растворитель может оказывать нивелирующее или дифференцирующее действие в отношении различных классов соединений. Дифференцирующее действие растворителей на электролиты обусловливается взаимодействием растворителя с электролитом, сопровождающимся образованием продуктов присоединения разной прочности. Чем более сильным акцептором протонов является растворитель, тем большим нивелирующим действием по отношению к кислотам он будет обладать. Поэтому в протофильных растворителях (например, в жидком аммиаке) значительно большее, чем в воде, число кислот будет сильным, а в протогенных растворителях (уксусная кислота) многие кислоты, сильные в воде, становятся слабее.
4. Буферные системы, их свойства. Расчет рН буферных растворов. Буферные растворырастворы с определенной концентрацией водородных ионов, содержащие сопряженную кислотно-основную пару, обеспечивающую устойчивость величины их водородного показателя при незначительных изменениях концентрации либо при добавлении небольшого количества кислоты или щелочи.Кислотно-основная пара Б. р. представляет собой слабую кислоту и ее соль, образованную сильным основанием (например, уксусная кислота СН3СООН и ацетат натрия CH3COONa) или слабое основание и его соль, образованную сильной кислотой (например, гидроокись аммония NH4OH и хлористый аммоний NH4CI). При разведении раствора или добавлении к нему некоторого количества кислоты или щелочи кислотно-основная пара способна соответственно быть донором либо акцептором водородных ионов, поддерживая т.о. величину водородного показателя на относительно постоянном уровне.Б.р. сохраняют устойчивость буферных свойств в определенном интервале значений рН, то есть обладают определенной буферной емкостью.Буферная емкость находится в прямой зависимости от концентрации Б. р.: чем концентрированнее раствор, тем больше его буферная емкость; разведение Б. р. сильно уменьшает буферную емкость и лишь незначительно изменяет рН.Буферные свойства проявляются очень слабо, если концентрация одного компонента в 10 раз и более отличается от концентрации другого. Поэтому буферный раствор часто готовят смешением растворов равной концентрации обоих компонентов либо прибавлением к раствору одного компонента соответствующего количества реагента, приводящего к образованию равной концентрации сопряженной формы. а)Кислые: Слабая кислота (НАс) +Соль(NaAc).HAc=H++Ac-.NaAc=Na++Ac-.Ka=[H+][Ac-]/[HAc] [H+]=Ka*[HAc][Ac-]=10-5*0,1/0,1=10-5. pH=5 б)основные: Слабое основание(NH4OH)+соль слабого основ.(NH4Cl). NH4OH=NH4++OH- NH4Cl=NH4++Cl-. Kb=[NH4+][OH-]/[NH4OH]. [OH-]=Kb*Cосн/Cсоли -lg[OH-]=-lgKb-lg Cосн/Cсоли. pOH=pKb-lg Cосн/Cсоли. pH=14- pKb+lgCосн/Cсоли
5. Равновесия в растворах комплексных соединений. Ступенчатое комплексообразование. Константы устойчивости и нестойкости комплексов, их взаимосвязь. Комплексным называют соединение,образующее в твердом состоянии кристаллическую решетку, узлы которой содержат комплексные ионы, способные существовать в растворе и расплаве.Например, соединение K[BiI4] является комплексным, а ион [BiI4] - комплексом, поскольку этот ион может быть получен из реальных частиц:Bi3+ + 4I- = [BiI4]- или BiI3 + I- = [BiI4]- В то же время сложное соединение KBiO3 не является комплексным, а ион BiO3- - комплексом, т.к. этот ион не может быть непосредственно получен из более простых частиц Bi3+ и O2- (ион O2- просто не существует в растворе).Координационная теория комплексных соединений разработана швейцарским химиком А. Вернером (1893 г.) и рассматривает терминологию комплексов и их составных частей по взаимному расположению частиц. Согласно этой теории комплексное соединение состоит из внутренней (собственно комплекса) и внешней сфер.
В зависимости от заряда комплекса КС подразделяют на: катионные - [Cu(NH3)4]Cl2, [Cr(H2O)6]Cl3; анионные - K2[Fe(CN)6], H[AuCl4], H2[SiF6]; катионно-анионные - [Pt(NH3)4][PbCl4] нейтральные комплексы (неэлектролиты) - [Co(NH3)4(NO3)2], [Pt(NH3)4Br3]. В растворах КС имеет место первичная и вторичная диссоциация (в расплавах КС происходит их термическая диссоциация). Первичная диссоциация протекает по типу сильных электролитов - практически необратимо: K4[Fe(CN)6] 4K+ + [Fe(CN)6]4-[Co(NH3)6]Cl3 [Co(NH3)6]3+ + 3Cl-. Первичной диссоциации не подвергаются комплексы без внешней сферы: [Pt(NH3)2Cl2], [Co(NH3)3(NO3)3]. Вторичная диссоциация характеризует диссоциацию самого комплекса. Она протекает в незначительной степени, подчиняется закону действия масс. Этот процесс характеризуют константой диссоциации. Так как величина этой константы фактически определяет прочность комплекса, то ее обычно называют константой нестойкости (K ). Вторичная диссоциация протекает по типу слабого электролита - обратимо и ступенчато:[Ag(NH3)2]+ [Ag(NH3)]+ + NH3, [Ag(NH3)]+ Ag+ + NH3В целях упрощения формы записи обычно записывают суммарное уравнение вторичной диссоциации:[Ag(NH3)2] Ag+ + 2NH3. Выражение константы нестойкости имеет вид:
Общая константа нестойкости комплекса равна произведению констант диссоциации по всем ступеням: Константа устойчивости относится к процессу образования комплексного иона и равна обратной величине константы нестойкости:β = 1/Кнест..Константа устойчивости характеризует равновесие образования комплекса.Значения констант нестойкости, приводимые в справочниках, используют для характеристики устойчивости комплексов, нахождения концентраций частиц (комплекса, комплексообразователя, лигандов) в растворе КС, для определения направленности химических реакций с участием комплексных соединений и др. Например, равновесие в реакции: [Ag(NH3)2]Cl + 2KCN = K[Ag(CN)2] + 2KCl + 2NH3будет смещено вправо, так как Kнест.([Ag(NH3)2]+) = 9,3·10-8, а Kнест.([Ag(CN)2]-) = 8,0·10-22, т.е. второй комплексный ион значительно прочнее первого: Процесс образования комплексных соединений протекает ступенчато:Ag+ + NH3[Ag(NH3)]+ ,β-константа образования.β=а[Ag(NH3)]+ /аAg+ *аNH3.[Ag(NH3)]+ + NH3[Ag(NH3)]+2. Ag+ + 2NH3[Ag(NH3)]+2.В зависимости от условий проведения реакции равнов-я описывается:1)термодинамическими:КТн,βТ.2)реальными:КРн, βР.3)условными: КУн, βУ.
Поиск по сайту: |
 В + Н+ (А - кислота, В - основание). Согласно этой теории кислотами являются молекулы или ионы, способные быть в данной реакции донорами протонов, а основаниями являются молекулы или ионы, присоединяющие протоны (акцепторы). Кислоты и основания получили общее название протолитов.Сущностью кислотно-основного взаимодействия является передача протона от кислоты к основанию. При этом кислота, передав протон основанию, сама становится основанием, так как может снова присоединять протон, а основание, образуя протонированную частицу, становится кислотой. Таким образом, в любом кислотно-основном взаимодействии участвуют две пары кислот и оснований, названные Бренстедом сопряженными: А1 + В2
В + Н+ (А - кислота, В - основание). Согласно этой теории кислотами являются молекулы или ионы, способные быть в данной реакции донорами протонов, а основаниями являются молекулы или ионы, присоединяющие протоны (акцепторы). Кислоты и основания получили общее название протолитов.Сущностью кислотно-основного взаимодействия является передача протона от кислоты к основанию. При этом кислота, передав протон основанию, сама становится основанием, так как может снова присоединять протон, а основание, образуя протонированную частицу, становится кислотой. Таким образом, в любом кислотно-основном взаимодействии участвуют две пары кислот и оснований, названные Бренстедом сопряженными: А1 + В2  А2 + В1.Одно и то же вещество в зависимости от условий взаимодействия может быть как кислотой, так и основанием (амфотерность). Например, вода при взаимодействии с сильными кислотами является основанием: H2O + H+
А2 + В1.Одно и то же вещество в зависимости от условий взаимодействия может быть как кислотой, так и основанием (амфотерность). Например, вода при взаимодействии с сильными кислотами является основанием: H2O + H+  H+ + OH–
H+ + OH– ,откуда [H+][OH–]=K[H2O]=Kw .
,откуда [H+][OH–]=K[H2O]=Kw .
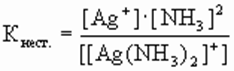

 .
.