|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Геометрические параметры АС ⇐ ПредыдущаяСтр 2 из 2
Именно благодаря наличию такой вещи, как водородная связь,вода может себе позволить образование ассоциативных структур. К таким структурам относят димер воды(2 вида), тример (), тетрамер(), …………… полимер воды.[6] Начиная с 80-х годов 20 века химиками – теоретиками по всему земному шару стало интересным влияние водородной связи в воде на её свойства – как физические так и химические! Благодаря очень быстрому развитию вычислительной техники и теории в квантовой химии уже в 1987 году стало возможным подсчитать энергию водородной связи с относительной ошибкой в 0.26%. Порой водный полимер в литературе называют водным кластером. Так первая статья, что посвещена изучению этих кластеров датируется 1991 годом. Кластеры воды представляют значительный самостоятельный интерес, их модели полезны для понимания поведения воды-мономера в конденсированных фазах.[6] Известно, что отвечающие глобальному минимуму энергии структуры водных кластеров (H2O)n {n=3–5} - циклические, в то время как при n>5 более энергетически выгодными являются трехмерные конфигурации.[7] Для октамера воды наиболее предпочтительны кубические конфигурации D2d и S4, то же самое дают MP2 и G3 расчеты.[7] Геометрические параметры кластеров (расстояние между атомами кислорода молекул, образу- ющих Н-связь, и отклонение валентного угла от угла мономера) находятся в хорошем соответствии с MP2 расчетами, а энергии связи совпадают практически идеально со значениями, полученными экстраполяцией энергий MP2 к пределу полного базиса и CCSD(T) (Burnham C.J., Xantheas S.S. J. Chem. Phys. 2002. V. 116. P. 5115–5124). Таким образом, можно утверждать, что расчет энергии связи методом B3LYP сравним с наиболее точными ab initio методами.
Рис. 8. Структуры водных кластеров n=2–8, соответствующие глобальным ми- нимумам энергии. C увеличением размера кластера длина водородной связи уменьшается, что свидетельствует об ее усилении. Этот факт отражает рост по абсолютной величине энергии H-связи (от димера к гексамеру энергия возрастает в 1.5 раза). Однако, эти зависимости имеют тенденцию к некоторому насыщению. [8]
Что касается энергии ассоциативных стуктур то тут гигантский вклад произвели [9],[10],[11],[15]. Плодом работы [9] есть ниже приведенная таблица с вычеслинными значениями энергии.
Первые теоретические исследования воды-димера опубликовали в 1968 году Morokuma и Pedersen. Димер и тример воды является темой горячего исследований в физической химии по нескольким причинам: 1. (Н2О)2 игратет важную роль во многих атмосферных процессов, включая кислотные дожди. 2. Кроме того именно длагодоря наличию димера в жидкой воде мы можем объяснить стольвысокую и точасти ономальную подвижность протона. В L. Gonzaleza, 0. MÓ, M. Yanez, J. Elguero провели гигантское исследоване по изучению геометрических параметров димера воды в довольно больших базасах.[9]
3.2. Спектральные параметры АС
В спектрах кластеров можно выделить три характерные области: 1. до 1000 см−1 межмолекулярные колебания кластеров: трансляционные (самые низкочастотные) и либрационные; 2. ∼ 1600–1680 см−1 деформационные колебания; 3. 3000–3750 см−1 валентные колебания. В большинстве случаев ИК интенсивность и КР активность валентных колебаний выше деформационных и межмолекулярных. [12] Для полосы антисимметричных колебаний частота больше в том случае, когда молекула является одиночным донором протона в Н-связи, нежели двой- ным. Напротив, в случае полос симметричных и деформационных колебаний частота выше для молекул двойных доноров протона. С увеличением размера кластера частота интенсивной моды коллективных симметричных колебаний испытывает красное смещение. В то же время антисимметричные моды свободной ОН-связи испытывают заметное красное смещение только при переходе мономер→димер→тример, а затем частота этих мод меняется незначительно и находится в районе 3710 см−1. Отличительной чертой спектров водных кластеров является сдвиг частот, полученных в гармоническом приближении, в низкочастотную область за счет ангармонизма. На рис. 3 представлено сравнение наиболее высокочастотной и низкочастотной (отвечающих антисимметричным и симметричным, соответ- ственно, валентным колебаниям молекул, образующих кластер) мод валентной полосы и высокочастотной моды полосы деформационных колебаний мономера, димера и циклических кластеров (H2O)n=3−6, вычисленных с учетом ангар- монизма, с результатами расчета MP2/aug-cc-pVDZ частот в гармоническом приближении. В среднем, ангармонический сдвиг для антисимметричных мод составляет 180, для симметричных — 147 и для изгибных — 36 см−1. [12] Рис. 10. Частоты некоторых валентных и деформационных колебательных мод мономера, димера и циклических водных кластеров n=3–6. Не прошли стороной они[9] и вопрос о частотах гармонического коллибания дмиера:
На Рис. 11 представлены экспериментальные спектры поглощения малораз-мерных водных кластеров в молекулярных пучках и рассчитанные ИК спектры (H2O)n=8,9. Из сравнения видно, что вычисленные частоты колебаний совпада- ют в пределах погрешности с наблюдаемыми линиями поглощения кластеров воды, таким образом примененный метод расчета спектров находится в хоро- шем согласии с экспериментом. Аномально высокая интенсивность свободных ОН-колебаний обусловлена, по всей видимости, присутствием в пучке свобод- ных молекул воды.[10] Был рассмотрен интегральный спектр комбинационного рассеяния под уг- лом 90 ◦ с вертикальной поляризацией падающего излучения в температурном интервале 20..80 ◦ C, и определена зависимость содержания кластеров от темпе- ратуры.[12]
Рис. 11. Экспериментальные и теоретические [(H2O)8: D2d и S4, (H2O)9)] ИК спектры октамеров и наномеров воды.
Оказалось, что тример и тетрамер воды доминируют в смеси во всем интер- вале температур. Концентрации тетрамера, пентамера и гексамера уменьшают- ся с ростом температуры, в то время как содержание димера и мономера растет.
Рис. 12. Зависимость содержания кластеров в смеси от температуры.[11]
Наиболее интенсивные спектральные линии тетрамера, пентамера и гексамера находятся в низкочастотной части валентной полосы, тогда как линии моно- мера, димера и тримера — в высокочастотной. Следовательно, интенсивность низко- и высокочастотного плечей ОН-полосы должна уменьшаться и увеличи- ваться, соответственно, с ростом температуры благодаря уменьшению концен- траций «тяжелых» кластеров (n=4–6) и увеличению концентраций «легких» кластеров (n=1–3), что полностью согласуется с экспериментом. Предложен- ная модель адекватно описывает зависимость контура ОН-полосы интеграль- ного КР спектра от температуры.[13.14]
Рис. 13. Рассчитанные интегральные и деполяризованные КР спектры (ОН- полоса) при разных температурах.
Аналогично сравнение проводилось с экспериментальными зависимостями, полученными при разных поляризационных условиях в температурных интер- валах 3..72 ◦C, -6..48 ◦C, -30..80 ◦C. И в этих случаях результаты расчета находятся в качественном согласии с экспериментальными данными. Небольшие отличия могут быть вызваны разницей в точности определения температур, экс- периментальных установках и исследуемых водных образцах. Примеси также могут оказывать влияние на спектр жидкой воды.[15,16]
7. КХ расчёты димера и тримеров воды
В эксперементальной части проводилось кваново-химические расчёты с помощью програмного комплекса «Gaussian.» Изходя из возможностей аппаратной части было выюрано 2 метода расчёта: 1. Hartree-Fock`s method. 2. MP2(Moller-Plesset perturbation theory) Для каждого метода Я выбрал один и тот же набор базисных наборов: 1. STO-3G. 2. 3-21G. 3. 6-311G. 4. 6-311G++. Каждый случай расчёта предпологал в себе минимизацию энергии, оптимизацию геометрии и вычисление частот коллибания. Результаты приведины ниже.
Молекула воды.
Рис.14. Общая – лптимизированная геометрия молекулы воды.
Рис.15. Дифформационное колибание молекулы
Рис.16. Валентное плоскостное.
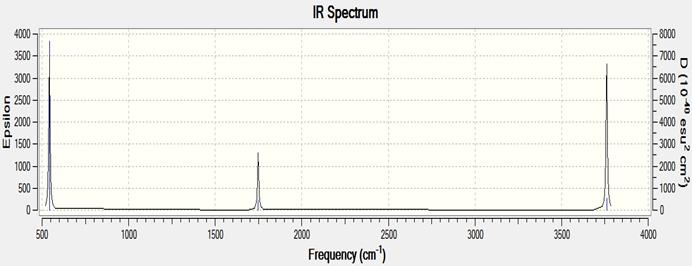
Рис.17. ИК спектр молекулы воды в MP2 6-311G++.
Ион гидроксония
Рис.18. Гидроксоний ион после оптимизации геометрии.
Коллибания иона гидраксония( MP2 for 6-311G++ basis): 542.22 cm-1 , 1747.71 cm-1 , 1747.71 cm-1 , 3570.33 cm-1 , 3760.27 cm-1 , 3761.06 cm-1 .
Рис.19. ИК спектр молекулы воды в MP2 6-311G++.
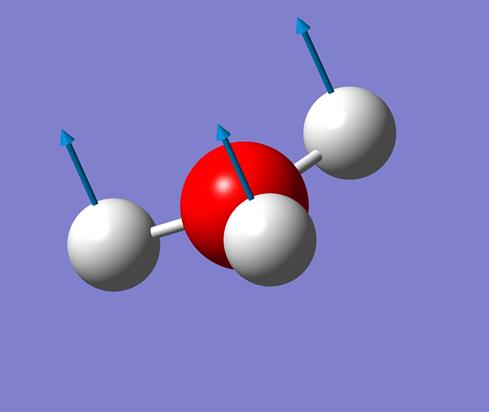
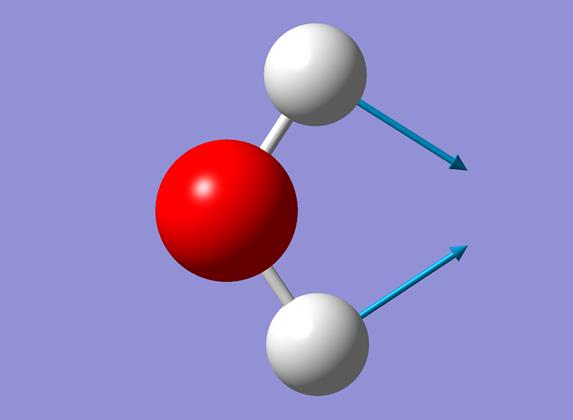
Рис.20. Вектор самых ситьных – диформационных колибаний. .
Рис.20.1. Вектор самых ситьных – диформационных колибаний. .
Димер воды
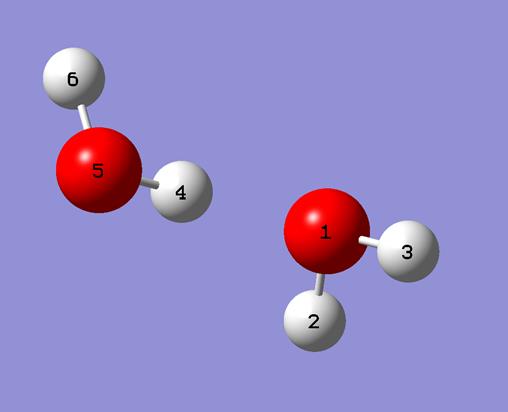
Рис.21. Возможные димеры воды.
Сразу хочится отметить: · При моделировании димера №2б в мометн оптимизации геометрии, он переходил в димер №1. Об этом свидетельствовало одинаковые длинны связей меж соответствующими атомами.(даже в низких базисах) · Была возможность опредиления частот колибания неровновесной структуры, но Я посчитал что это будет просто глупо и ненужно! · Энергия димера №2 была больше чем у димера №1 (во всех случаях) что и говорит о том что эта структура есть более нестабильная чем димер №1.
Геометрические характеристики димера №1:
Рис.22. ИК спектр молекулы воды в MP2 6-311G++.
Коллибания иона гидраксония( MP2 for 6-311G++ basis): 141.04 cm-1 , 209.15 cm-1 , 225.59 cm-1 , 235.26 cm-1 , 402.28 cm-1 , 822.96 cm-1 ,1641.66 cm-1 , 1645.51 cm-1 , 3542.08 cm-1 , 3667.11 cm-1 , 3791.57 cm-1 , 3883.53 cm-1 .
Тример воды
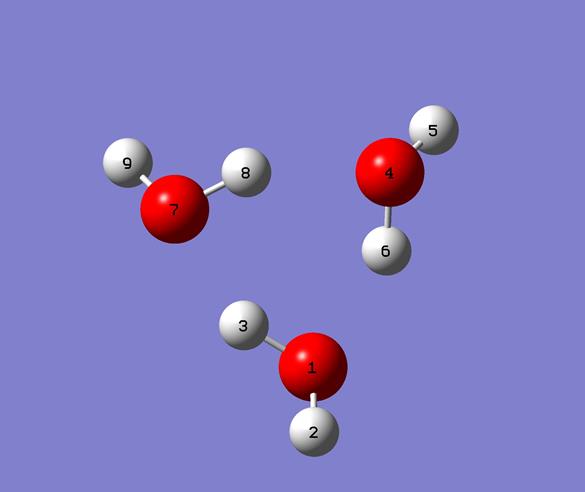
Рис.23. Возможные тримеры воды.
Рис.24. Самый устойчивый тример воды.
Рис.24..1 Самый устойчивый тример воды.
Сразу хочится отметить: · При моделировании тримера №1 и №2 в мометн оптимизации геометрии, они переходил в тримера№3. Об этом свидетельствовало одинаковые длинны связей меж соответствующими атомами.(даже в низких базисах) · Была возможность опредиления частот колибания неровновесной структуры, но Я посчитал что это будет просто глупо и ненужно! · Энергия тримера №1 и № 2 были больше чем у тримера №3 (во всех случаях) что и говорит о том что эта структура есть более нестабильная чем тример №3.
Геометрические характеристики тримера №3 (MP2 for 6-311G++ basis):
Частоты коллибаний в тримере № 3 226.5 cm-1 , 255.12 cm-1 , 285.45 cm-1 , 290.95 cm-1 , 310.19 cm-1 , 332.61 cm-1 , 492.83 cm-1 , 508.95 cm-1 , 657.08 cm-1 , 846.14 cm-1 , 967.59 cm-1 , 1264.95 cm-1 , 1836.05 cm-1 , 1852.67 cm-1 , 1882.52 cm-1 , 3446.11 cm-1 , 3573.71 cm-1 , 3579.54 cm-1 3921.33 cm-1 , 3924.87 cm-1 ,3927.8 cm-1 .
Обсуждение результатов.
Что касается результатов расчёта водородной связи то результаты имеют очень хороший отклик с [9] и [11] , где говорится что с ростом количества молекул в ассоциате энергия водородной сязи становится более отрицательной(в таблице энергия водородной связи по модулю)
Что касается коллибаний димера и триемера по отношению к отправной точек – одной молекулы воды, то тут можно сказать что в следствии присоединения новых молекл к мономеру наблюдается появление новых частот в диапазоне от 1600 до 3800 см-1. Эти «предельные частоты» определены собственным валентым и дифформ. коллибание молекулы воды, а то что меж ними – те новые колибание что возможны е новом ассоциате.
Выводы.
1. C увеличением размера кластера длина водородной связи уменьшается, что сви- детельствует об ее усилении. Этот факт отражает рост по абсолютной величине энергии H-связи.
2. С увелисение количества молекул в ассоциате появляются новые частоты коллибания в «предельном пороге» и нетолько.
3. Геометрия что соответстует самому стабильному тримеру воды есть ничто иное как «шести членный цикл» из 3 атомов водорода и 3 атомов кислорода. Все 6 атомов в одной плоскости.
Литература 1.http://ru.wikipedia.org/wiki/Вода . 2.http://bse.sci-lib.com/article005846.html. 3.Пиментел Дж., Мак-Клеллан О. Водородная связь. М.: Мир, 1964. 462 с. 4.Шахпаронов М.И. Межмолекулярные взаимодействия. М.: Знание, 1983. 64 с. 5.Денисов Г.С., Соколов Н.Д. Водородная связь // Химическая энциклопедия. М.: Сов. энциклопедия, 1988. Т. 1. С. 403-404. 6.http://www.scopus.com/home.url 7.Structural changes of hydrogen bonded hexagonal trimers upon ionization. 8.Two-dimensional model treatment of torsional motions in the water trimer. 9.Cooperative effects in water trimers. The performance of density functional approaches. 10.External electric field effects on the water trimer. Clifford E. Dykstra. Chemical Physics Letters: Volume 299, Issue 2, 6 January 1999, Pages 132-136 11.Water dimer vibration–rotation tunnelling levels from vibrationally averaged monomer wavefunctions.Ross E.A. Kellya, Jonathan Tennysona, Gerrit C. Groenenboomb and Ad van der Avoirdb. Journal of Quantitative Spectroscopy and Radiative Transfer: Volume 111, Issue 9, June 2010, Pages 1262-1276. 12.Карговский А.В. Водные кластеры: структуры и оптические колеба- тельные спектры. Изв. вузов. Прикладная нелинейная динамика 2006. Т. 14 No 5. C. 122-131. 13.The vibrational spectrum of the water trimer: Comparison between anharmonic ab initio calculations and neon matrix infrared data between 11,000 and 90 cm−1 . 14.Kargovsky A.V. On temperature dependence of the valence band in the Raman spectrum of liquid water. Laser Phys. Lett. 2006. V. 3. No 12. P. 567–572. Published online: 1 September 2006 at http://dx.doi.org/10.1002/ lapl.200610063 15.Formation of water dimers in expanding air flows. Sylwia Ptasi ska, Józef D bek and Leszek Michalak.Vacuum: Volume 70, Issues 2-3, 10 March 2003, .Pages 403-409. 16.Electron capture dynamics of the water dimer: a direct ab initio dynamics study. Hiroto Tachikawa. Chemical Physics Letters: Volume 370, Issues 1-2, 7 March 2003, Pages 188-196. Ebeling W., Kargovsky A., Netrebko A., Romanovsky Yu. Fermi Resonance — New Applications of an Old Effect. Fluct. Noise Lett. 2004. V. 4. No 1. P. 183–193.
Поиск по сайту: |














 )
)