|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Основные медиаторы альтерации
III. Механизмы экссудации. Сосудистые и внесосудистые реакции при воспалении.
Основные медиаторы экссудации
Экссудация с нарушением микроциркуляции и эмиграцией I. Сосудистые реакции: 1. Ишемия - ангиоспастическая кратковременная (из-за разрушения адреналина и норадреналина под влиянием МАО и КОМТ), возможна обтурационная вследствие тромбоза.
2. Артериальная гиперемия обуславливает развитие одного из классических признаков воспаления (rubor) - красноты. Возможны все механизмы артериальной гипеперемии.
3. Смешанная гиперемия.
4. Венозная гиперемия – повышение проницаемости капилляров ® скопление жидкости в интерстиции ® сдавление венул и лимфатических капилляров. Классический признак - отек (tumor). Последствия: § Сгущение крови и повышение вязкости. § Активация гемостаза, адгезия и агрегация форменных элементов (монетные столбики, сладж), образование микротромбов, изменение физико-химических свойств крови, появление в крови некоторых белков (глобулины острой фазы), понижение альбумин-глобулинового коэффициента. § Маргинация (краевое стояние) лейкоцитов. § Набухание эндотелиальных клеток.
5. Стаз способствует гиперкоагуляции и тромбозу; возможны все виды стаза.
II. Собственно экссудация Экстравазация жидкости из-за увеличения проницаемости сосудистой стенки. Другими словами происходит: § Разрушение стенки сосудов при альтерации. § Округление эндотелиальных клеток и появление межклеточных щелей (гистамин, брадикинин). § Микровизикуляция эндотелия - эндоцитоз и трансцитоз компонентов плазмы. § Раздвигание эндотелиальных клеток лейкоцитами по типу “расстёгивание молнии”. § Увеличение фильтрационного давления и площади фильтрации. Различают раннюю экссудацию, 5-30 мин. (действие биогенных аминов и ацетилхолина на посткапиллярные венулы) и позднюю экссудацию, от 1 часа до 7 суток (действие полипептидных и липидных медиаторов на венулы и капилляры). Также происходит выход форменных элементов. Отличием экссудата от транссудата является наличие более 2-3% белка.
III. Эмиграция 1. Экстравазация форменных элементов - маргинация лейкоцитов, которая объясняется § изменением заряда поврежденных клеток, § фиксацией в межэндотелиальных щелях - “ловушках”, § движением с током жидкости, § образованием мостиков, § влиянием медиаторов (фибронектин, компоненты системы комплемента, XII фактор, каллекреин, брадикинин).
2. Движение лейкоцитов через сосудистую стенку. Лимфоциты и моноциты проникают через эндотелиальные клетки, не повреждая их. Полиморфноядерные лейкоциты - через эндотелиальные щели.
3. Движение клеток из сосуда в очаг воспаления по градиенту хемотаксинов называется хемотаксисом, в случае если это движение без градиента и беспорядочно - хемокинез. Способность привлекать в очаг воспаления лейкоциты называется хемоаттракцией, ею обладают хемоаттрактанты: § Различные цитокины. § Микроорганизмы и их продукты. § Система комплемента и др. компоненты контактной системы. § Некротаксины - деграданты коллагена, фибронектин (гной лейкоцитов). § Иммунные комплексы, некоторые медиаторы (гистамин для эозинофилов). Хемоаттрактанты воспринимаются рецепторами лейкоцитов. Движение лейкоцитов обеспечивается структурами цитоскелета: микрофиламетами и микротрубочками. При участии Са++ и Са-связывающего белка гельзолина, актина цитоскелета. Желатинизация актина сопряжена с сокращением элементов цитоскелета.
Виды экссудатов: 1. Серозный (на слизистой - катаральный). 2. Фибринозный (крупозный и дифтерический на слизистой ротовой полости). 3. Гнойный. 4. Гнилостный. 5. Геморрагический (из-за анаэробов). 6. Хилёзный (за счёт жира из лимфатической системы брюшной полости).
IV. Стадии и механизмы фагоцитоза. Причины незавершенного фагоцитоза. Методы фармакологической коррекции фагоцитоза.
Стадии фагоцитоза 1. Приближение (случайное и хемотаксис). Основныее медиаторы хемотаксиса
2. Контакт, распознавание и прилипание. В процессе распознавания большую роль играет опсонизация - это покрытие объекта фагоцитоза сыворочными факторами - опсонинами (антителами IgG, М и Е, они «метят» объекты, подлежащие элиминации). Прилипание осуществляется посредством связи опсонинов с рецепторами фагоцитов. Завершенный фагоцитоз идет только с участием опсонинов.
3. Поглощение (механизм: псевдоподии ® фагосомы ® фаголизосомы). При поглощениее живых микроорганизмов,последние сначала должны быть убиты. В лейкоцитах существует 2 бактерицидных механизма: § зависящий от кислорода; § независящий от кислорода.
Зависящий от кислорода бактерицидный фактор связан с образованием активных метаболитов кислорода. Продукция этих веществ начинается после контакта фагоцитов с опсонизированными бактериями. Именно в это время фагоциты, которые в обычных условиях используют энергию анаэробного гликолиза, начинают усиленно поглощать кислород, что обозначают термином респираторный взрыв. Возникновение его обусловлено активацией цитопламатической НАДФН-оксидазы, которая катализирует одноэлектронное восстановление молекулы кислорода до супероксидного радикального аниона, «отбирая» электрон от восстановленного пиридинового нуклеотида НАДФН:
оксидаза 2О2 + НАДФН ¾¾¾® 2О2- + НАДФ+ + Н+.
Расходуемые во время «респираторного взрыва» запасы НАДФН начинают немедленно восполняться усиленным окислением глюкозы через гексозомонофосфатный шунт. Большая часть образующихся при восстановлении О2 супероксидных анионов О2- подвергается дисмутации до Н2О2:
2О2- + 2Н+ ¾® О2 + Н2О2.
Некоторая часть молекул Н2О2 взаимодействует в присутствии железа или меди с супероксидным анионом с образованием чрезвычайно активного гидроксильного радикала ОН·:
О2- + Н2О2 ¾® ОН· + ОН- + О2.
Цитоплазматическая НАДФ·Н-оксидаза активируется в месте контакта фагоцита с микробом, а образование супероксидных анионов происходит на внешней стороне мембраны лейкоцитов, вне внутренней среды клетки. Процесс продолжается и после завершения образования фагосомы, вследствие чего внутри нее создается высокая концентрация бактерицидных радикалов. Проникающие внутрь цитоплазмы фагоцита радикалы нейтрализуются ферментами супероксиддисмутазой и каталазой. Система образования бактерицидных метаболитов кислорода действует во всех профессиональных фагоцитах. В нейтрофилах совместно с ней действует еще одна мощная бактерицидная система – система миелопероксидазы (сходная с ней пероксидазная система имеется также у эозинофилов, но ее нет у моноцитов и макрофагов). Миелопероксидаза - фермент, содержащийся в азурофильных гранулах нейтрофилов, катализирует реакцию между ионом галогена (обычно хлора) и перекисью водорода, что приводит к образованию хлорноватистой кислоты (гипохлоритного аниона ОС1-):
миелопероксидаза CI- + Н2О2 ¾¾¾¾¾¾¾¾® OCI- + Н2О.
Гипохлорит оказывает выраженное бактерицидное действие сам по себе. Кроме того, он может реагировать с аммонием или аминами, образуя бактерицидные хлорамины. Независящий от кислорода бактерицидный механизм связан с дегрануляцией - поступлением внутрь фагосомы бактерицидных веществ, которые содержатся во внутриклеточных гранулах фагоцитов. Когда образование фагосомы завершается, к ней вплотную приближаются гранулы цитоплазмы фагоцитов. Мембрана гранул сливается с мембраной фагосомы, и содержимое гранул вливается внутрь фагосомы. Полагают, что стимулом к дегрануляции является увеличение цитозольного Са2+, концентрация которого возрастает особенно сильно вблизи фагосомы, где располагаются органеллы, накапливающие кальций. Цитоплазматические гранулы всех облигатных фагоцитов содержат большое количество биологически активных веществ, способных убивать и переваривать микроорганизмы и другие поглощенные фагоцитами объекты. В нейтрофилах, например, имеется 3 типа гранул:
Наиболее легко мобилизуемые секреторные пузырьки облегчают выход нейтрофилов из сосудов, их миграцию в тканях. Уничтожают и разрушают поглощенные частицы вещества азурофильных и специфических гранул. В азурофильных гранулах, помимо уже упомянутой миелопероксидазы, содержатся действующие независимо от кислорода низкомолекулярные бактерицидные пептиды дефенсины, слабое бактерицидное вещество лизоцим и множество разрушающих ферментов; в специфических гранулах лизоцим и белки, останавливающие размножение микроорганизмов, в частности, лактоферрин, связывающий необходимое для жизнедеятельности микроорганизмов железо. На внутренней мембране специфических и азурофильных гранул находится протонный насос, который переносит водородные ионы из цитоплазмы фагоцита внутрь фагосомы. В результате рН среды в фагосоме понижается до 4-5, что вызывает гибель многих находящихся внутри фагосомы микроорганизмов. После того как микроорганизмы погибают, они разрушаются внутри фагосомы с помощью кислых гидролаз азурофильных гранул. К числу важных бактерицидных факторов, действующих в активированных макрофагах, следует отнести и продукцию оксида азота (NO), которая осуществляется с помощью индуцибильной NO-синтазы. Фермент этот активируется g-интерфероном, фактором некроза опухолей, ИЛ-1 и другими воспалительными цитокинами. NO действует цитостатически на опухолевые клетки, бактерии, паразиты, вирусы, ингибируя активность многих ферментов, участвующих в синтезе белков и нуклеиновых кислот. Оксид азота может соединяться с О2-, образуя пероксинитрит, который распадается на цитотоксические свободные радикалы ОН· и NO-.
4. Переваривание за счёт сильных эндогенных окислителей и ферментов, таких как гидролазы, комплемент, лизоцим, аргиназа.
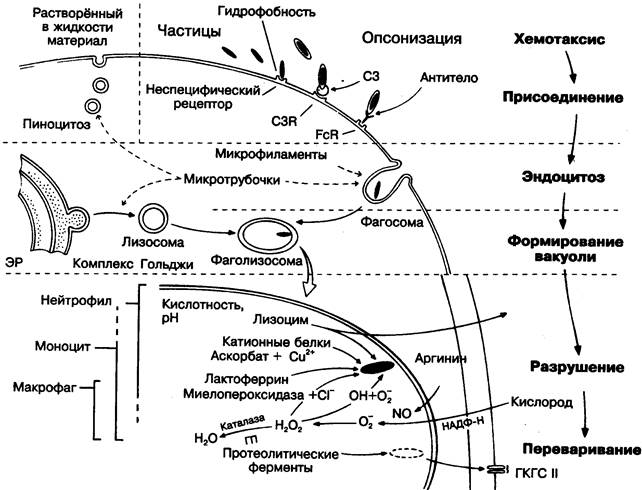
Рис. 10.4. Схема фагоцитоза.
Некоторые микроорганизмы (микобактерии, трипаносомы, листерии, сальмонеллы) ингибируют образование фаголизосом, и возбудители персистируют в фагоците. Они сохраняются, оказываясь при этом «отгороженными» мембраной и цитоплазмой фагоцитов от противомикробных лекарств. Последняя (4-я) стадия фагоцитоза не развивается, формируется незавершенный фагоцитоз.
Причины незавершенного фагоцитоза: 1. Дефицит белка. 2. Дефицит витаминов. 3. Наследственные ферментопатии. 4. Иммунодефициты. 5. Особенности возбудителя (его размеры значительно превышают размеры самого фагоцита). 6. Объектом фагоцитоза являются комплексы антиген-антитело, находящиеся на плоской поверхности сосудистого эндотелия.
Как следствие, раздраженные мононуклеары выделяют монокины, лимфокины, которые стимулируют хемотаксис, соседние клетки соединительной ткани и др. Активированные хемоаттрактантами фагоциты способны высвобождать содержимое своих гранул не только внутрь фагосомы, но и во внеклеточное пространство. При этом содержимое гранул и продуцируемые фагоцитами активные метаболиты кислорода воздействуют и на объект атаки, и на ткани организма хозяина. Дистантно развивается лейкоцитоз.
При затяжных воспалительных процессах (сопровождающихся незавершенным фагоцитозом) целесообразно применять
§ путем искусственного обострения воспаления, вводя, например, искусственно получаемые эндотоксины бактерий (продигиозан); § через активацию лимфоцитов иммуностимуляторами (см. тему "Патология иммунитета").
Поиск по сайту: |