 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Нуклеофільними1 (такими, що шукають ядра) називають реагенти, які віддають електронну пару при утворенні хімічного зв'язку із субстратом.
До нуклеофільних реагентів належать аніони і нейтральні молекули, які містять атоми з неподіленими парами електронів або центри з підвищеною електронною густиною.
ОСнОВи теОрІЇ реаКЦІЙ ОрГанІЧних СПОЛУК
1) іони, які несуть негативний заряд (аніони): ОН , СІЧ", КО , ІЧН2, 2) нейтральні молекули, які містять одну або кілька неподілених пар електро 3) молекули, які мають центри з підвищеною електронною густиною (алкени,
Нуклеофіли здатні утворювати ковалентний зв'язок із субстратом, атакуючи в його молекулі центри зі зниженою електронною густиною. Електрофільними1 (такими, що шукають електрони) називають реагенти, що приймають електронну пару від субстрату при утворенні з ним хімічного зв'язку. До електрофільних реагентів належать катіони і нейтральні молекули, які мають вакантну орбіталь або центри зі зниженою електронною густиною. Типові електрофільні реагенти: 1) іони, які несуть позитивний заряд (катіони): протон (Н+), катіони металів 2) нейтральні молекули, які мають вакантну орбіталь: SO3, кислоти льюїса 3) молекули, які мають центри зі зниженою електронною густиною: галогено- похідні вуглеводнів (-,С—Наї), сполуки з карбонільною групою С С 6+С° 6+С-° 6+С-° К—СГ , К—СГ , К—СГ , К—СГ , К—СГ тощо, ХН ХК' ХОН ХОК' хНа1 а також галогени2 Cl2, Br2, I2. електрофільні реагенти здатні утворювати ковалентний зв'язок із субстратом, атакуючи в його молекулі центри з підвищеною електронною густиною. електрофільні і нуклеофільні реакції, подібно до процесів окиснення і відновлення, нерозривно пов'язані між собою, тобто залежно від того, яка з реагуючих речовин приймається за атакуючий реагент, а яка — за субстрат, ту ж саму реакцію можна назвати як електрофільною, так і нуклеофільною. Однак найчастіше субстратом вважають речовину зі складнішою структурою або речовину, молекули якої надають атом Карбону для утворення нового зв'язку. Крім гомо- і гетеролітичних, відомі реакції, які перебігають зa так званим пе-рициклічним (молекулярним) механізмом. Молекулярний механізм характеризується одночасним (узгодженим) розривом і утворенням зв'язків у реагуючих молекулах. Молекулярні реакції проходять без утворення іонів або радикалів. Вони супроводжуються синхронним переміщенням електронів у субстраті і реагенті. Типовим прикладом молекулярної реакції є приєднання дієнів до алкенів:
2 Галогени виявляють електрофільні властивості під дією Глава 8 116 Г
Поиск по сайту: |
 Від лат. писіеш — ядро і грец. сріХіа (філіа) — дружба, любов.
Від лат. писіеш — ядро і грец. сріХіа (філіа) — дружба, любов. Типові нуклеофільні реагенти:
Типові нуклеофільні реагенти: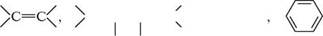
 1 Від грец. Т|Хєкхроу — електрон і срйш — дружба, любов.
1 Від грец. Т|Хєкхроу — електрон і срйш — дружба, любов.