|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Фізико-хімічні, біохімічні основи процесуСтр 1 из 5Следующая ⇒
ВСТУП На сьогодні велика увага приділяється лікуванню захворювать печінки. По оцінкам експертів ВООЗ в світі вірусом гепатита інфіковано близько 2 мільярдів чоловік. Кожний рік первинно заражаються більше 50 млн людей. Найбільш ефективним і економічно-доцільним фармацевтичним препаратом при лікуванні печінки є Цитраргінін. Цитраргінін – це об`єднання двох компонентів природного походження: аргініна і бетаіна. Аргінін – амінокислота, яка бере участь в біосинтезі білка, способствує виділенню кінцевих продуктів розпаду білка, підвищує детоксикаційну функцію печінки. Аргінін володіє антиокидатними властивостями , покращує мікроциркуляцю печінки. Бетаін – ліпотропна речовина, яка бере участь в біосинтезі фосфоліпідів, окисленні і метаболізмі ліпідів. Способствує попередженню і зменшенню жирової дистрофії печінки. Іони цитрата позитивно впливають на процеси травлення. Після прийому препарату аргінін метаболізується з утворенням орнітина. Орнітин оприділяється в високій концентрації в плазмі крові і тканинах печінки. Бетаін розприділяється, безпосередньо, в печінці та почках. У біотехнологічній промисловості комплексній механізації і автоматизації надається велика увага. Це пояснюється складністю і високою швидкістю протікання технологічних процесів, а також чутливість їх до порушення режиму, шкідливість умов роботи. Автоматизація обраного процесу приводить до поліпшення основних показників ефективності виробництва: збільшенню кількості, поліпшенню якості і зниженню собівартості продукції, що випускається, підвищенню виробництва праці. Упровадження автоматичних пристроїв забезпечує високу якість продукції, скорочення браку і відходів, зменшення витрат сировини і енергії, зменшення чисельності основних робітників, зниження капітальних витрат на будівництво будівель, подовження термінів міжремонтного пробігу устаткування. Упровадження спеціальних автоматичних пристроїв сприяє безаварійній роботі устаткування, виключає випадки травматизму, попереджає забруднення атмосферного повітря і водоймищ промисловими відходами. Тому автоматизацію технологічного процесу розроблено на основі Рlant Scape.
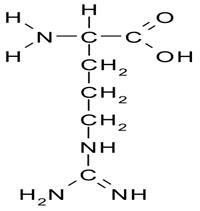
Фізико-хімічні, біохімічні основи процесу Аргінін (δ-гуанідин-α-аміновалеріанова кислота, скорочення Арг, Arg, R) — основна α-амінокислота, l-форма якої входить до 20 амінокислот, що становлять основу білків. Для людини аргінін є напівнезамінною амінокислотою, тобто біохімічні шляхи для її біосинтезу існують, проте в певні періоди життя, зокрема інтенсивного росту та розвитку, а також під час деяких захворювань вони не можуть забезпечувати достатньої кількості цієї сполуки, через що вона повинна потрапляти в організм із їжею. Для деяких видів тварин, таких як птахи, хижі та морські ссавці, аргінін є незамінною амінокислотою. Окрім того, що аргінін входить до складу білків, ця амінокислота також важлива для багатьох інших метаболічних шляхів клітини, зокрема синтезу нітроген (II) оксиду, поліамінів, проліну, глутамату, креатину та агматину. Емпірична формула аргініну - C6H14N4O2. Структурна формула аргініну:
В кислих і нейтральних середовищах аргінін існує переважно як катіон (форма I, II), здатний утворювати сполуки по амінній групі. В лужному середовищі він існує у вигляді аніона (форма IV). В сильнополярних розчинниках аргінін існує у вигляді цвітер-іону (форма III). Тому аргінін розчинний в розведених мінеральних кислотах і може утворювати з ними солі. Крива титрування аргініну має три точки перегину і представлена на рисунку 1. Крива титрування - це графік залежності pH, оптичної щільності або яких-небудь інших характеристик титруємого розчину від обсягу до даного титранту .
Рисунок 1 – Крива титрування аргініну Таблиця 1 - Хімічні властивості аргініну
Значення рІ основних амінокислот вичисляють як середнє арифметичне значення рК2 і рК3, наприклад для аргініну рІ= (8,99 + 12,48) / 2 = 10,76. Значення рК характеризує кислотність амінокислот. [Якубке]. Аргінін є основною амінокислотою, яка несе два основних центра: аміногрупу в α-положенні і гуанідинову групу в δ -положенні. Гуанідинова група завдяки резонансній делокалізації заряду є основною (pKa 12.48), знаходиться в протонованій катіонній формі при pH < 10 і здатна утворювати множинні водневі зв'язки. У слаболужних і нейтральних розчинах аргінін утворює цвіттер-іон. Висока основність аргініну і, відповідно, здатність утворювати іонні зв'язки з фосфатними групами ДНК, зумовлює утворення нуклеопротеїдів. L- Аргінін зустрічається в багатьох продуктах харчування, як тварини, так і рослинного походження. У таблиці наведені дані по вмісту аргініну на 100 грам продукту і зазначено вміст білка.
Бетаїн - ліпотропна речовина, яка бере участь у біосинтезі фосфоліпідів, окисленні і метаболізмі ліпідів. Сприяє попередження та зменшення жирової дистрофії печінки. Емпірична формула бетаїну - С5Н11NО2, молярна маса – 117,148 г/моль. Структурна формула:
Бетаїн - форма сполук, що містить карбоксильну групу і четвертинний атом N, іноді третинні атоми S або О; відносяться до цвітеріонів. Залежно від положення атома N (S або О) щодо карбоксильної групи розрізняють – бетаїн α, β, γ. Бетаїн має високу температуру плавлення, зазвичай добре розчинний у воді, погано - в ефірі. При нагріванні до 300°С бетаїн N- метильованих амінокислот перетворюються на метилові ефіри. Бетаїн γ амінокислот при нагріванні утворює лактон і третинний амін. З солями важких металів (Pb , Au , Pt ) бетаїн утворює нерозчинні в органічних розчинниках комплекси, з НСI - гідрохлориди.
Перетворення амінокислот в бетаїн шляхом їх повного метилювання – процес характерний для азотистого обміну багатьох рослин і тварин. Бетаїн гліцину виділений з цукрового буряка (Beta vulgaris), триптофану (гіпафорин) - з Erythrino hypaphorus, проліну (стахідрин ) - з Stachys tuberifera, Betonica oficinalis, γ аміномасляної кислоти (γ бутиробетаїн) - з гнилого м'яса. Синтетичний бетаїн містить вуглеводневі радикали С10 - С18, - амфотерні поверхньо активні речовини, які використовуються в якості емульгаторів. У числі біологічно активних сполук , що підвищують поживну цінність кормів для птиці, за кордоном використовується бетаїн. Як менш дорогий компонент, він служить замінником синтетичного холіну (вітамін В4) і частково, - метіоніну. Бетаїн також представляє інтерес як регулятор жирового обміну та як речовина, що підвищує життєздатність і продуктивність птиці при захворюваннях різної природи. За хімічною структурою бетаїн являє собою триметилгліцин - похідне найпростішої амінокислоти гліцину. Він зустрічається у всіх живих організмах, будучи проміжним продуктом процесу переметилювання. Холін, що надходить з кормом в травний тракт птиці, піддається дегідруванню і перетворюється в бетаїн. У молекулі бетаїну є три активні метильні групи (СНЗ -) , які необхідні для цілого ряду ключових процесів обміну речовин. Приєднання метильної групи (метилювання) є обов'язковим етапом найважливіших біохімічних реакцій. Введення в корм тварин натурального метил-донора бетаїну дозволяє обмежити використання синтетичних джерел метильних груп.
Поиск по сайту: |