 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
НЕНАСИЧЕНІ МОНОКАРБОНОВІ КИСЛОТИ
До ненасичених карбонових кислот належать карбонові кислоти, які містять у вуглеводневому радикалі кратний зв'язок. Залежно від взаємного розміщення кратного зв'язку і карбоксильної групи розрізняють сс-Р, р-у та інші ненасичені кислоти. НОМЕНКЛАТУРА ТА ІЗОМЕРІЯ У номенклатурі ненасичених кислот широко застосовують тривіальні назви. За замісниковою номенклатурою ШРАС назви ненасичених кислот утворюють аналогічно насиченим, додаючи су- !'»''___________ .... (Ьікс -єн (-єн) для позначення подвійного зв'язку, суфікс -ии (-і«) — пдя позначення потрійного, указуючи положення кратного зв'яз-^ Б карбоновому ланцюзі. Назви деяких ненасичених монокарбо-ноВих кислот наведено у табл. 18.4. Таблиця 18.4 Назви деяких ненасичених монокарбонових кислот
н2£=сн-соон Н2с=с-соон
СНз Н2с=сн-сн2-соон Н^ = /СООН Н-с=<Н НзСГ" ^СООН НС=С—СООН Н3С—С^С—СООН н3с нс=сн соон
\сн2і7 (сн2{7 н3с нс=сннс=сн соон \снХ <4 }сн2{7 Для ^^^2°^°^^^^^^ мерія, що пов'язана з різним розмиценням замісників вщнос площини подвійного зв'язку. н7с^н-сн2-соон н3с-сн=сн-соон п2^ ч_-п^іа2 о-бугенова кислота 3-бутенова кислота
Чис-2-бутенова кислота транс-2-бутенова кислота 18.2.2. СПОСОБИ ДОБУВАННЯ ». Для добування ненасичених монокарбонових кислот існує ба4 гато методів синтезу насичених карбонових кислот. Як вихідні реї човини застосовують ненасичені сполуки, наприклад, окиснення ненасичених первинних спиртів і альдегідів за м'яких умов, гідр&І ліз нітрилів та ін. Крім того, вдаються до специфічних методів. Гідрокарбоксилування алкінів (реакція Реппе). У присутності карбонілів металів алкіни взаємодіють з карбон (II) оксидом у водному середовищі з утворенням а, Р-ненасичених монокарбоч нових кислот: N1,(00)4 но^сн + со + н2о ~—*■ н2с=сн—соон акрилова кислота Елімінування Р-галоген- і р-гідроксикарбонових кислот. р-Гало-генкарбонові кислоти при нагріванні з водою відщеплюють гало-геноводень і перетворюються на а, Р-ненасичені кислоти: сн2—сн2—соон Лі р-хлоропропіонова кислота р-Гідроксикарбонові кислоти при нагріванні відщеплюють молекулу води і перетворюються на а, Р-ненасичені кислоти: СН2—СН2—СООН Дтт (5-гідроксипропіонова кислота МоНокар^оновм<ислоти^ Зі збільшенням молекулярної маси кислоти розчинність у воді ^еНшується. Вищі ненасичені кислоти нерозчинні у воді, але добре розчиняються в органічних розчинниках. ХІМІЧНІ ВЛАСТИВОСТІ реакційна здатність ненасичених монокарбонових кислот зумовлена наявністю в їх структурі карбоксильної групи і кратного зв'язку. За рахунок карбоксильної групи ненасичені кислоти вступають у реакції, характерні для насичених кислот, зокрема вони утворюють солі, галогенангідриди, ангідриди, естери, аміди (див. розд. 18.1.4). По кратному зв'язку у вуглеводневому радикалі ненасичені кислоти виявляють властивості алкенів (алкінів). Так, для них характерні реакції приєднання, окиснення та полімеризації (див. розд. 10.6). Проте приєднання галогеноводнів до а,Р-не-насичених кислот, в яких кратний зв'язок знаходиться в спряженні з карбоксильною групою, відбуваетея всупереч правилу Марковникова. Це пояснюється електроноакцепторним впливом карбоксильної групи за рахунок -М- та -7-ефекгів:
£
н2с=-сн^< * й-♦ ? \>н і
Ненасичені кислоти, особливо з .по^ій™^'™в^нТми більш виражені кислотні властивості поршняно *™™2ш1 рахунок делокалізаци заряду ™ «читаними порівняння наведено значення рК у воді (при.я»УЛ« сичених карбонових кислот та ?Ка прошонової кислоти.
За звичайних умов ненасичені монокарбонові кислоти є безбарвними рідинами або кристалічними речовинами. Нижчі представники добре розчинні у воді, мають різкий подразливий запах- Н,С—СН2—СООН; рКа = 4,87 Н,С- О^С—СООН; рКа = 2,60 НС=СН—СООН; рКа = 4,26 нс^с—соон рКа = 1,84
Карбонові кислоти. Глава ОКРЕМІ ПРЕДСТАВНИКИ Акрилова кислота СН2=СН—СООН.Безбарвна рідина з рі| ким запахом (т. пл. 13 °С, т. кип. 141 °С), добре розчиняєтьсЯ у воді. Акрилова кислота легко полімеризується з утворенням паїліакрилової кислоти. Важливе практичне значення мають поліме-1ри на основі естерів акрилової кислоти — так звані поліакрилатиі О
...4сн2—сн—I- (Ж
поліакрилат ІІ У медицині поліакрилати знаходять застосування у виготовленні зубних протезів.
Метакрилова кислота.Безбарвна рідина (т. кип. 160,5 °С), лег
соосн,
соосн,
з *-"з метилметакрилат поліметилметакрилат
\
Монокарбонові кислоти
Поиск по сайту: |
 Формула
Формула
 18.2.3. ФІЗИЧНІ ВЛАСТИВОСТІ
18.2.3. ФІЗИЧНІ ВЛАСТИВОСТІ




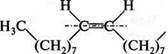 Олеїнова кислота (цис-9-октадеценова кислота) СН3—(СН2)7—СН=СН—(СН2)7—СООН.Безбарвна масляниста рідина без смаку та запаху. У вигляді естерів гліцерину входить до складу рослинних олій. Особливо багато її міститься в маслиновій, мигдальній та соняшниковій оліях. Олеїнова кислота є цис-ізомером. При дії нітроген (IV) оксиду 1Ч02 олеїнова кислота ізомеризується в ела'щинову кислоту, яка є /и/ганс-ізомером:
Олеїнова кислота (цис-9-октадеценова кислота) СН3—(СН2)7—СН=СН—(СН2)7—СООН.Безбарвна масляниста рідина без смаку та запаху. У вигляді естерів гліцерину входить до складу рослинних олій. Особливо багато її міститься в маслиновій, мигдальній та соняшниковій оліях. Олеїнова кислота є цис-ізомером. При дії нітроген (IV) оксиду 1Ч02 олеїнова кислота ізомеризується в ела'щинову кислоту, яка є /и/ганс-ізомером: >Ю2(Си + конц. НІМО3)
>Ю2(Си + конц. НІМО3)