 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Конденсированные системы
Рассмотрим, какие ещё упорядоченные системы спонтанно формируются в мезомире – мире большого скопления молекул при достаточном плотном их расположении ( конденсированном состоянии вещества). Это состояние соответствует расстоянию между молекулами, при котором существенны электромагнитные силы, т.е. не более, чем 10-6 м. Как правило, главной причиной, вынуждающей молекулы сблизится на такое расстояние, является гравитационное взаимодействие. В частности, на Земле конденсированное состояние вещества обусловлено силой тяжести – силой гравитационного притяжения Земли. Сблизившись на такое расстояние, молекулы начинают взаимодействовать электромагнитными силами друг с другом. Это взаимодействие носит сложный характер [16,45 ], так как обусловлено подвижностью электронных оболочек молекул. Это приводит к формированию более упорядоченных, чем газ, агрегатных состояний – жидкому и твердому. Переход от хаотического (газообразного) состояния к жидкому сопровождается уменьшением энтропии на величину
где ΔQпар и Тпар – теплота и температура парообразования (конденсации). Внешне бόльший порядок жидкости по сравнению с газом выражается в четко обозначенной границе, отделяющей объём этой жидкости от других объектов. Сама граница может изменять свою конфигурацию, но величина объема при этом не меняется. Переход от жидкого состояния к твердому приводит к ещё большей упорядоченности, так как граница отвердевшего объекта не меняется. При этом энтропия уменьшается на величину
где ΔQпл и Тпл – теплота и температура плавления (кристаллизации). Порядок твердого тела характеризуется двумя факторами: 1) неизменностью геометрической конфигурации границы (естественно, при отсутствии внешнего воздействия), 2) неизменностью расстояний между молекулами (кристаллическая структура). Очень важным фактором увеличения упорядоченности, связанным с фазовыми переходами от газа к жидкости, и от жидкости к твердому телу, является уменьшение объема вещества – увеличение его плотности. Как было указано выше (§2.2), увеличение плотности вещества (количества молекул в единице объема) свидетельствует о количественном увеличении порядка, так как уровень неопределённости расположения частицы в меньшем объеме ниже, чем в большем. Тепловая энергия, выделяемая при конденсации газа и кристаллизации жидкости, приводит к нагреву окружающих объектов, т.е. к повышению их энтропии. Сама по себе эта энергия берется за счет уменьшения потенциальной энергии электромагнитного взаимодействия молекул преобразуемого вещества. Следовательно, формирование упорядоченных агрегатных состояний вещества является следствием двух перечисленных в §2.1 тенденций – повышения энтропии и понижения потенциальной энергии. Кроме перечисленных трех агрегатных состояний, конденсированное вещество может находится еще в нескольких видах. Перечислим некоторые из них. Жидкие кристаллы: Жидкости, образованные веществом с длинными молекулами, содержащими несколько десятков атомов. Хотя поверхность объектов, образованных жидкими кристаллами, легко видоизменяется под действием внешних факторов, сами молекулы расположены и двигаются друг относительно друга не хаотически, а по ограниченному числу траектории. Это обстоятельство, во-первых, создает анизотропные свойства вещества. (Например, неодинаковый коэффициент преломления при прохождении электромагнитной волны под разными углами). Во-вторых, эта анизотропность может видоизменяться внешними полями. Гели: псевдорастворы некоторых твердых веществ также с длинными молекулами, в которых эти молекулы притягивают к себе молекулы растворителя. Внешне такие гели образуют полужидкость, полутвердое тело (например, желе). Чаще всего из вещества в таком состоянии состоят живые организмы. Протоплазма клеток состоит, как правило, из 70÷90% воды и 30-10% белка (полимеров аминокислот). Молекулы белка представляют собой длинную нить, свёрнутую в клубок (глобулу), окружённый оболочкой, состоящей из молекул воды, притянутых к наружным мономолекулам клубка (см. §6.3). Плазмы: полужидкое, полугазообразное состояние, состоящее из “обломков” молекул – ионов. Например: пламя, электрическая дуга, молния, искры, Солнце, звезды. Аморфные вещества: вещества, внешне имеющие главный признак твердого – неизменную границу, но при этом хаотическое (некристаллическое) расположение молекул. Примеры: стекло, бумага, картон, некоторые полимерные материалы. Особыми формами конденсированного состояния вещества являются растворы, сплавы, взвеси, коллоиды, химические соединения. Наружная часть атмосферы Земли окружена магнитосферой [17,26,45 ] – еще одной разновидностью конденсированного состояния. В космическом пространстве обнаружены объекты с весьма своеобразной формой конденсации – нейтронные звезды, черные дыры. Несмотря на всё разнообразие конденсированных состояний вещества, каждое из них является более упорядоченным, чем состояние идеального газа. Причем механизм его формирования также определяется сформулированными в предыдущей главе необратимыми тенденциями.
Неравновесные системы Для того, чтобы возникли перечисленные выше упорядоченные агрегатные состояния конденсированного вещества, необходимо, чтобы существовали объекты, температура которых ниже, нежели исходная температура того множества молекул, которое принимает это состояние. Дело в том, что в природе тепловая энергия может передаваться только от объекта большей температуры объекту меньшей температуры. Это обстоятельство является прямым следствием второго начала термодинамики. Действительно, рассмотрим два тела: 1 – с температурой Т1, 2 – с температурой Т2<T1 (рисунок 3.4). Если первое тело теряет количество тепловой энергии ΔQ1, то изменение его энтропии отрицательное
Зато энтропия второго тела положительная, так как оно получает тепловую энергию ΔQ2=ΔQ1:
Суммарная энтропия этих двух тел возросла:
Ясно, что если бы передача тепловой энергии от первого тела второму не происходила, то изменение энтропии было бы равно нулю. Если бы теплота передавалась от 2 к 1, то изменение энтропии было бы отрицательным. И то, и другое противоречит второму началу термодинамики. Когда на пути передачи теплоты от более нагретого тела к менее нагретому расположено третье тело, то в нём возможны процессы, связанные с уменьшением энтропии, т.е. процессы упорядочивания. Действительно, пусть часть тепловой энергии ΔQ1 теряется в этом третьем теле О (рис. 3.5) в виде энергии W0.Тогда теплота ΔQ2становится равной ΔQ2 = ΔQ1 - W0.
Энтропия движения молекул в теле О может быть отрицательной, если соблюдается условие
Рис. 3.4 Появление отрицательной энтропии при передаче тепловой энергии
Действительно, эта энтропия ΔS0 складывается из двух
и может быть меньше нуля при сформулированном выше условии (3.4). В формуле (3.5) теплота ΔQ1имеет знак плюс, так как поступает в тело О, а ΔQ2– минус, так как передается телу 2.
Рис. 3.5. Термодинамически неравновесная система трёх тел: 1 - источник тепловой энергии; 2 - холодильник; 0 - открытая система.
Как видим, при наличии объектов с разными температурами возможно формирование упорядоченных структур из хаотических, но при одном обязательном условии – часть тепловой энергии обязательно должна быть передана объекту с низкой температурой. Такие процессы и соответствующие им системы именуются неравновесными. Следует подчеркнуть, что эти процессы естественные и формируют порядок, гармонию в ограниченной области пространства. Причем движущей силой их служит энтропия, т.е. присущая всем природным явлениям тенденция к хаотическому движению. Главная особенность неравновесной системы – устойчивое существование в условиях непрерывного производства отрицательной энтропии (гармонии). В нашей повседневной жизни мы непрерывно сталкиваемся с такими системами. Это, во-первых, все живые организмы и биосистема в целом. Это, во-вторых, все, что создано творчеством человека, в первую очередь, индустрия. Это, в-третьих, большинство явлений неживой природы на земле. Обобщенно элементы неравновесной системы именуются [2, 3, 12, 86] следующим образом: 1-источник тепловой энергии (или просто источник энергии), 2 – акцептор тепловой энергии (или просто холодильник), 0 – открытая система. Ясно, что главным элементом неравновесной систем являются открытая система, так как именно в ней формируется порядок. Ещё раз отметим, что тепловое, хаотическое движение в открытой системе может преобразоваться в упорядоченное (механическое, гидравлическое, аэродинамическое, электрическое, химическое и т.п.) только под воздействием базисных физических полей. По сути дела, эти процессы и системы и являются совокупным "творцом" всего того многообразного в своей гармонии мира. Необыкновенно красивые кристаллы, причудливые исполины – горы, фантастическая архитектура пещер, реки, озера, моря, закаты и восходы, айсберги, голубое небо и радуга, полярное сияние, громы и молнии, снег и дожди, звезды и метеориты, вулканы и горячие источники – все это можно перечислять до бесконечности. Диссипативные системы Чем больше разность температур Т1 и Т2, тем большая величина информации (отрицательной энтропии) поступает в открытую систему. При определенном значении информации в открытой системе происходит качественный скачок – упорядоченное движение в ней становится сложным – в нём появляется новая закономерность, новое свойство. Так, например, если система О в схеме рисунка 3.5 представляет собой объём с газом, то конвекция в нём, вызванная разностью температур (Т1 – Т2), с увеличением этой разности протекает всё с большей и большей скоростью. После достижения этой скоростью определённого значения ламинарная циркуляция газа превращается в турбулентную. Молекулы газа по- прежнему двигаются коллективно, но не поступательно, а по сложным поступательно-вращательным (вихревым) траекториям [70]. Открытая система распадается на две части (рисунок 3.6): 1)рабочий агент и 2) диссипативная система. Рабочий агент – это такая часть открытой системы, в которой тепловое (хаотическое) движение превращается в простое упорядоченное. Диссипативная система – такая часть открытой системы, в которой простое упорядоченное движение превращается в сложное. Обе части не обязательно пространственно отделены друг от друга. В случаях, когда они совмещены, передачу тепловой энергии в холодильник производит сама диссипативная система. Отсюда название: передача теплоты в холодильник (чаще всего – окружающую среду) во многих отраслях естественных и технических наук именуется рассеянием (диссипацией). Иногда диссипативную систему именуют далёкой от равновесия неравновесной[6, 8, 16], подчеркивая тем самым, что сложный порядок возникает при достаточно большом различии между температурами Т1 и Т2.
Рисунок 3.6 Структура неравновесной системы, включающей в себя диссипа- тивную систему
Следует отметить, что объекты рисунка 3.6 могут быть отделены друг от друга не только в пространстве, но и во времени. Тогда в качестве рабочего агента выступает объект, аккумулирующий энергию, которую он затем передает в диссипативную систему. Так, например, в роли рабочего агента может выступать химическое соединение, когда-то аккумулировавшее в себе тепловую энергию Солнца или остывающей Земли, а теперь выделяющее его при сгорании в каком-нибудь механизме или живом организме. Наличие источника больших количеств энергии с большой температурой и необъятного холодильника с температурой, близкой к нулю, создает ситуацию непрерывной передачи энергии упорядоченного движения в диссипативную систему. Такая ситуация сложилась, например, на Земле. В качестве источника выступает Солнце, а в качестве холодильника – космическое пространство. Согласно [1,68], на 1м2 земной поверхности попадает 1010 Дж солнечной радиации (по всему частотному спектру – от инфракрасного до g- лучей) в год. Эта энергия соответствует [49] потоку информации 6´1014 Вт / 0К на всю поверхность Земли или 1023 байт на 1 м2 ежесекундно. Иными словами, единица поверхности Земли получает в единицу времени порядок в количестве, превышающем информационную ёмкость всех существующих компьютеров. Неудивительно, что на Земле сформировался и продолжает накапливать гармонию весьма высокоразвитый, т. е. очень сложный по своей структуре природный феномен. Ниже будем рассматривать, как происходит развитие природы, т. е. непрерывное усложнение ее структуры, в этой уникальной зоне – Земле. При этом следует подчеркнуть, что удельная тепловая энергия, поступающая от Солнца на единицу поверхности ближайших к Земле планет – Венеры и Марса – соответственно больше и меньше, чем первой, в 2 ÷ 2,5 раза. Это оказалось вполне достаточно, чтобы сложившиеся на этих планетах условия не смогли обеспечить формирование такой сложной биосферы, как на Земле. В роли рабочего агента выступают, в частности: - двигатель автомобиля (диссипативная система – вся его ходовая часть, включая органы управления); - аккумуляторная батарея (или просто батарейка) многочисленных бытовых устройств: мобильных телефонов, портативных радиоприемников, фонариков, калькуляторов и др.; - сеть электропитания бытовых устройств (пылесосов, холодильников, печей «Электроника», ламп и т.д.); электротранспорта, станков и другого промышленного оборудования; - митохондрии клеток.
Поиск по сайту: |

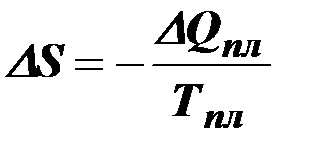




 (3.4)
(3.4) (3.5)
(3.5)