 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
К определению величины стандартного электродного потенциала меди ⇐ ПредыдущаяСтр 2 из 2
Внимание! Учитывая высокую токсичность солей меди металлов, все отработанные растворы не сливаются в раковину, а сдаются лаборанту для последующей утилизации. 3. Определение ЭДС химического гальванического элемента. (Медно – цинковый гальванический элемент). В соответствии со схемой, представленной на рис 2, соберите установку для определения ЭДС гальванического элемента, составленного из цинкового и медного электродов при стандартных условиях.
Рис.2 Схема установки для определения ЭДС химического гальванического элемента: 1 – медный электрод, 2 – цинковый электрод 3 - электролитический ключ ( стаканчик с раствором хлорида калия), 4 - потенциометр. В соответствии с инструкцией о порядке измерений с использованием соответствующего потенциометра, определите ЭДС данного гальванического элемента Э.Д.С.(Сu|CuSO4||Zn|ZnSO4)эксп. Сравните полученное в эксперименте значение с расчетным (теоретическим) значением ЭДС для медно - цинкового гальванического элемента: ЭДС (Сu|CuSO4||Zn|ZnSO4)теорет. = E катода –Е анода = = E0(Cu+2/Cu0) - E0( Zn+2/Zn0) = 0,34 – (– 0,76) = 1,1B. Полученные данные занесите в табл3 . Таблица 3 К определению величины электродвижущей силы Медно-цинкового гальванического
Напишите уравнения и назовите процессы, протекающие на катоде и аноде данного гальванического элемента при его работе. Таблица 4 Потенциалы электродов сравнения
Поиск по сайту: |
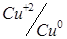 ) по хлор - серебряному насыщ..
) по хлор - серебряному насыщ..
 ).
).
