 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Удельная электропроводность растворов. Эквивалентная электропроводность растворов ⇐ ПредыдущаяСтр 2 из 2
Проводники электрического тока делятся: 1)Проводники 1-го рода (металлы): ток переносится путём направленного движения электронов. Движение тока не приводит к химическим изменениям. 2)Проводники 2-го рода ( твёрдые соли, концентрированные расплавы и растворы электролитов): при повышении температуры возрастает проводимость, т.к. уменьшается процесс гидратации ионов и вязкость среды. Примем движение ионов, за движение шариков в вязкой среде. На них действует сила среды, пропорциональная силе поля: Количественной способностью проводника проводить электрический ток, является удельная электропроводимость (c) – электропроводимость объёма электролита, помещённого между электродами (S=1см2 ) на расстоянии 1 см:
Электродные процессы. Двойной электрический слой. К электродным процессам относится:1)Процессы, где создаётся разность потенциалов между частями системы. Из-за перехода электронов от одного атома к другому возникает электрический ток. 2)Обратные предыдущим, протекающие в результате электролиза (из-за действия тока протекает химическая реакция). При погружении металла в растворитель, происходит переход атомов металла в виде ионов в растворитель. Через некоторое время устанавливается равновесие между числом атомов металла, переходящих в раствор, и ионов металла, осаждающихся на поверхности пластины – двойной электрический слой. ГЭ и цепи. Разность между зарядами данного слоя, наз-ся разностью потенциалов: Факторы, влияющие на величину скачка При замыкании системы, происходит нарушение равновесия системы из-за перехода электронов.В результате возникновения разности потенциалов, протекает самопроизвольный процесс – гальванический элемент, который является источником тока. Гальванический цикл – последовательность всех скачков φ, возникающих на поверхности раздела фаз, отвечающих данному гальваническому элементу. Гальванический элемент работает обратимо при: 1)Если его ЭДС на б.м.в. превышает приложенную из вне и противоположно направленную. 2) Если ε из вне на б.м.в. будет больше ε гальванического элемента. ЭДС является мерой убыли свободной энергии Гиббса реакции: Используя уравнение Вант-Гоффа и подставив значение ЭДС из уравнения (1), получаем математическое уравнение Нернста: Факторы:1)Природа материала электрода;2)Температура;3)Активность ионов металла.
Поиск по сайту: |
 . При увеличении скорости, увеличивается сопротивление среды:
. При увеличении скорости, увеличивается сопротивление среды:  ,
,  ,
,  , V – скорость иона,
, V – скорость иона,  - абсолютная скорость движения иона.
- абсолютная скорость движения иона.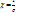 Зависит от:1)Природы электролита;2)Концентрации ионов электролита;3)Скорости движения;4)Вязкости среды;5)Величины диэлектрической постоянной растворителя;6)Температуры.
Зависит от:1)Природы электролита;2)Концентрации ионов электролита;3)Скорости движения;4)Вязкости среды;5)Величины диэлектрической постоянной растворителя;6)Температуры.
 : 1)Природа металла;2)Концентрация ионов металла в растворе электролита;3)Характер взаимодействия ионов с растворителем.
: 1)Природа металла;2)Концентрация ионов металла в растворе электролита;3)Характер взаимодействия ионов с растворителем. (1)
(1)