 |
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Определение скорости химической реакцииСтр 1 из 5Следующая ⇒
Химическая кинетика ХИМИЧЕСКАЯ КИНЕТИКА(от греч. kinetikos-движущий) – раздел химии, изучающий протекание химической реакции во времени, механизм этого процесса, его зависимость от внешних условий. Химическая кинетика (ХК) устанавливает временные закономерности протекания химических реакций, связь между скоростью реакции и условиями ее проведения, выявляет факторы, влияющие на скорость и направление химических реакций. Определение механизма сложного химического процесса позволяет выяснить, из каких элементарных стадий он состоит и каким образом элементарные стадии связаны друг с другом, какие образуются промежуточные продукты и т. п. Теоретическая химическая кинетика занимается построением математических моделей сложных химических процессов, анализом этих моделей в сопоставлении с экспериментальными данными. Важной задачей химической кинетики является изучение элементарных реакций с участием активных частиц: свободных атомов и радикалов, ионов и ион-радикалов, возбужденных молекул и др. Используя результаты кинетических исследований и изучения строения молекул и хим. связи, химическая кинетика устанавливает связь между строением молекул реагентов и их реакционной способностью. Основные понятия и определения Объектом изучения ХК является химическая реакция, протекающая в определенном временном интервале. Поскольку реакция представляет собой превращение одних веществ в другие, определим основные кинетические параметры реакции. Количественной характеристикой вещества является его концентрация, очевидно, что в ходе реакции концентрация исходных веществ должна убывать, а продуктов возрастать. Химическую реакцию можно представить как последовательность элементарных актов превращения веществ. Элементарным химическим актом является единичный акт взаимодействия частиц (молекул, радикалов, ионов, атомов и др.), в результате, которого, образуются новые частицы продуктов реакции или промежуточных соединений, при этом в одном элементарном акте может претерпевать единовременное изменение определенное число частиц (от 1 до 3). Вид элементарного акта определяет механизм реакции. Если все элементарные акты одинаковы, то считается, что реакция протекает в одну стадию и называется простой. Таких реакций относительно немного. Чаще всего реакция протекают в несколько стадий по одному или разным механизмам, в этом случае она является сложной. Изменение концентрации участников реакции во времени определяется кинетическим уравнением. Виды химических реакций Итак, все химические процессы по кинетическим параметрам можно разделить на простые и сложные. По пространственной области взаимодействия – на гомогенные (протекающие в объеме) и гетерогенные (протекающие на поверхности). Простые реакции. Молекулярность Все простые реакции бывают трех видов, различающихся по молекулярности. Молекулярность элементарной реакции — число частиц, которые, согласно экспериментально установленному механизму реакции, участвуют в элементарном акте химического взаимодействия. Мономолекулярные реакции — реакции, в элементарном акте которой происходит химическое превращение одной молекулы (изомеризация, диссоциация и т. д.) примером такой реакции является термическая диссоциация газообразного иода: I2 → 2I Бимолекулярные реакции — реакции, элементарный акт которых осуществляется при столкновении и изменении природы двух частиц (одинаковых или различных): СН3Вr + КОН → СН3ОН + КВr Тримолекулярные реакции — реакции, элементарный акт которых осуществляется при столкновении и превращении трех частиц: О2 + NО + NО → 2NО2 Реакции с молекулярностью более трёх неизвестны. Сложные реакции Сложные реакции – это многостадийные процессы. Механизм сложной реакции обычно представляют в виде схемы элементарных реакций. При изучении каждой реакции в кинетике решают две задачи: прямую и обратную. Прямая задача кинетики заключается в математическом описании закономерностей сложной реакции как многостадийного процесса, в котором каждой стадии соответствует своя константа скорости и для которого заданы начальные условия процесса. Обратная задача кинетики в узком смысле заключается в том, чтобы в рамках предложенной схемы на основании экспериментальных данных о процессе и характеристик некоторых его стадий оценить константы скорости отдельных стадий процесса. В широком смысле обратная задача может быть сформулирована как реконструкция схемы сложного процесса на основании данных об отдельных стадиях и знании кинетики процесса в целом. Реальное исследование включает последовательное решение прямой и обратной задач с промежуточным анализом результатов каждого этапа. В основе кинетики сложных реакций лежит принцип независимости отдельных стадий. Согласно этому принципу, если в системе протекает несколько реакций, каждая из них идет независимо от другой и подчиняется закону действующих масс. Полное изменение в системе является суммой изменений, внесенных всеми этими независимыми реакциями. Математически это означает, что кинетическое уравнение сложной реакции представляет собой алгебраическую сумму кинетических уравнений составляющих ее простых реакций. Этот принцип справедлив не всегда, в частности он неприменим для сопряженных реакций. 6.1.2.
Формальная кинетика
Определение скорости химической реакции Скорость химической реакции — изменение количества вещества одного из реагирующих веществ за единицу времени в единице реакционного пространства. Более точно скорость реакции определяется числом элементраных актов протекающих в единицу времени в единице объема для гомогенных реакций или на единице поверхности для гетерогенных:
Понятие скорости является ключевым в химической кинетике. На практике скорость химической реакции удобнее определять по изменению концентрации реагирующих веществ при этом если измерения проводятся за конечный промежуток времени то получают среденее значение скорости: , величина всегда положительная, поэтому, если она определяется по исходному веществу (концентрация которого убывает в процессе реакции), то отношение изменения концентрации к изменению времени берется со знаком минус. Более точное мгновенное значение скорости представим в виде производной:
Поиск по сайту: |
 Структура темы
Структура темы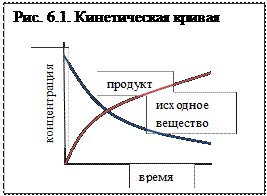 Формальная кинетика решает задачу определения основных кинетических параметров из экспериментальных данных. Обычно, при изучении кинетики химических реакций экспериментально получают кинетическое уравнение (кривую) из анализа которого определяется, какая реакция протекает – сложная или простая. Наиболее часто вид кинетической кривой представляет собой монотонно убывающую во времени концентрацию исходного вещества, или возрастающую продукта (рис.6.1.). Из кинетической кривой определяется скорость реакции в определенном временном интервале.
Формальная кинетика решает задачу определения основных кинетических параметров из экспериментальных данных. Обычно, при изучении кинетики химических реакций экспериментально получают кинетическое уравнение (кривую) из анализа которого определяется, какая реакция протекает – сложная или простая. Наиболее часто вид кинетической кривой представляет собой монотонно убывающую во времени концентрацию исходного вещества, или возрастающую продукта (рис.6.1.). Из кинетической кривой определяется скорость реакции в определенном временном интервале. – гомогенная реакция (6.1)
– гомогенная реакция (6.1) – гетерогенная реакция (6.2)
– гетерогенная реакция (6.2)