|
|
|
Архитектура Астрономия Аудит Биология Ботаника Бухгалтерский учёт Войное дело Генетика География Геология Дизайн Искусство История Кино Кулинария Культура Литература Математика Медицина Металлургия Мифология Музыка Психология Религия Спорт Строительство Техника Транспорт Туризм Усадьба Физика Фотография Химия Экология Электричество Электроника Энергетика |
Тема 6. Асиміляція вуглеводів мікроорганізмами
6.1 Основні відомості про асиміляцію вуглеводів
Обмін вуглеводів покликаний задовольняти три основні потреби клітини: 1) одержання енергії; 2) утворення попередників, необхідних для синтезів; 3) створення окислювально-відновних механізмів для перетворення цих попередників у відповідні проміжні або кінцеві продукти, які можуть бути використані як клітинні компоненти. Вуглеводи вводять у середовища у вигляді чистих цукрів, з яких частіше інших застосовують глюкозу, сахарозу, лактозу або технічні продукти, багаті вуглеводами, наприклад гідрол, який представляє собою маточний розчин після кристалізації глюкози, крохмаль (як технічний, так і той, що входить до складу борошна, дерті і т.п. ), мелясу. Всі вони містять переважно гексози, звичайно у вигляді полімерів. При використанні відходів гідролізного виробництва в середовищах присутні пентози. В останні роки в якості компонентів середовища застосовують молочну сироватку, яка містить лактозу. Якщо вводять відходи рослинних продуктів, зокрема буряковий гніт, то в них присутні уронові кислоти. Іноді компонентами середовищ є багатоатомні спирти, наприклад маніт. Незважаючи на розмаїтість можливих вуглеводів, що є присутніми у середовищах, всі вони вступають на шлях, характерний для катаболізму глюкози. Є ферментативні механізми, які здійснюють цей процес. Тому звичайно, коли розглядають шляхи включення вуглеводів у метаболізм клітини, як вихідний продукт приймають глюкозу. Відомі три шляхи асиміляції глюкози: 1) гліколіз; 2) гексозомонофосфатний шлях (пентозний, пентозофосфатний);
Рисунок 6.1- Шлях асиміляції глюкози по Ентнеру—Дудорову
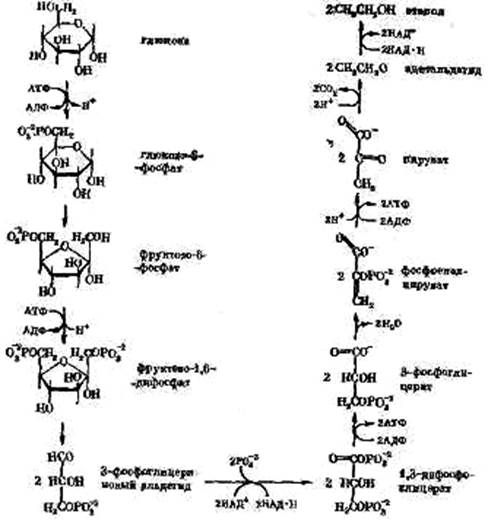
3) шлях Ентнера-Дудорова, який часто називають КДФГ-шлях по наявності характерного для нього продукту обміну - 2-кето-3-дезокси-6-фосфоглюконової кислоти (рис. 6-1). Перші два шляхи здійснюються практично у всіх промислово важливих мікроорганізмів, що відносяться як до прокаріотів, так і до еукаріотів. Гліколіз являє собою сукупність анаеробних ферментативних процесів розпаду глюкози. Біологічне значення гліколізу полягає в тім, що в результаті розпаду вуглеводів утворюються багаті енергією фосфорні з'єднання й речовини, використовувані для синтезу, а також є основними субстратами для окислювання. Один з головних субстратів окислювання - піровиноградна кислота (рис. 6.2).
Рисунок 6.2 - Зброджування глюкози, або гліколіз
6.2 Гексозомонофосфатний шлях
Інший шлях асиміляції глюкози на відміну від анаеробного - окисний, центральною ланкою якого є утворення пентоз (рис. 3.3), тому цей шлях називають пентозним. Пентозний, або гексозомонофосфатний, шлях метаболізму глюкози відіграє істотну роль у реакціях синтезу. Особливе значення пентозний шлях має у формуванні циклічних структур, зокрема азотмістких. До основних функцій циклу відносять наступні: 1) він поставляє відновлений НАДФ, необхідний для синтетичних процесів; 2) постачає енергію при повнім окислюванні всіх відновлених молекул НАДФ (на одну молекулу окисленої глюкози утворюється 36 молекул АТФ); 3) здійснює взаємоперетворення гексоз і пентоз. Пентозний шлях звичайно функціонує одночасно із гліколітичним. У результаті їхньої взаємодії створюються можливості для оборотних взаємоперетворень трьох-, чотирьох-, п'яти-, шести- і семивуглецевих цукрів шляхом оборотного переносу глікоальдегідних або диоксиацетонових груп. Перша реакція пентозного шляху здійснює дегідрування першого вуглецевого атома глюкозо-6-фосфата, яке каталізується глюкозо-6-фосфатдегідрогеназою. У результаті утворюються 6-фосфоглюконо-6-лактон і НАДФ-Н. Лактон гідролізується лактоназою до 6-фосфоглюконата. На наступній стадії 6-фосфоглюконат піддається окисному декарбоксилюванню при участі 6-фосфоглюконат-дегідрогенази, у результаті утворюється D-рибулозо-6-фосфат. Ця реакція супроводжується утворенням ще однієї молекули НАДФ-Н. При участі ізомерази й епімерази виникають ксилулозо-5-фосфат і рибозо-5-фосфат. Далі транскетолазна реакція приводить до утворення седогептутулозо-7-фосфата й гліцеральдегід-3-фосфата. Транскетолаза, що містить пов'язаний з нею кофермент тіамінпірофосфат, здійснює перенос глікоальдегідної групи від D-ксилулозо-5-фосфата до D-рибозо-5-фосфату. У цьому процесі глікоальдегідна група спочатку переноситься від D-ксилулозо-5-фосфата до пов'язаного з ферментом тіамінпірофосфату;
Седогептулозо-7-фосфат і гліцеральдегід-3-фосфат у результаті дії трансальдолази утворюють фруктозо-6-фосфат і еритрозо-4-фосфат. У трансальдолазній реакції відбувається перенос диоксиацетонової групи до D-гліцеральдегід-3-фосфату:
Седогептулозо D-гліцеральдегід D-фруктозо- D-эритрозо- -7-фосфат -3-фосфат 6-фосфат -4-фосфат
Рисунок 6.3 - Схема асиміляції глюкози по гексозомонофосфатному шляху
Повторювана транскетолазна реакція між ксилулозо-5-фосфатом й еритрозо-4-фосфатом приводить до утворення фруктозо-6-фосфата і гліцеральдегід-3-фосфата - характерних продуктів гліколітичного шляху розпаду вуглеводів. 3-фосфогліцериновий альдегід, ізомеризуючись у діоксиацетонфосфат, дає з останнім під дією фруктозобіфосфат-альдолази фруктозо-1,6-дифосфат. Гексозодифосфатаза перетворює фруктозо-1,6-дифосфат у фруктозо-6-фосфат:
Глюкозофосфатізомераза перетворює останній у глюкозо-6-фосфат. У результаті функціонування пентозного шляху з 6 молекул глюкозо-6-фосфата, що вступили в реакцію, утворюється п'ять молекул фруктозо-6-фосфата, які ізомеризуються в п'ять молекул глюкозо-6-фосфата. Підсумкове рівняння:
Сильним інгібітором гексозоізомеразної реакції є еритрозо-4-фосфат. Отже, якщо в системі ферментів пентозного шляхи утворилися проміжні продукти гліколізу (фруктозо-6-фосфат і гліцеральдегід-3-фосфат), то перетворення фруктозо-6-фосфата в глюкозо-6-фосфат виключене доти, поки є присутнім еритрозо-4-фосфат, і подальші перетворення фруктозо-6-фосфата можуть іти лише гліколітичним шляхом. Винятково важливе значення має механізм перемикання асиміляції глюкози з одного шляху на іншій. Одним з регулюючих факторів, що направляють глюкозу на шлях гліколізу, або пентозофосфатний шлях, є присутній у середовищі фосфат. Його надлишок гнітить активність глюкозо-6-фосфат-дегидрогенази, ключового ферменту пентозофосфатного циклу, а тому замість 6-фосфоглюконата в результаті активності фосфо-гексозоізомерази утвориться фрунтозо-6-фосфат. У такий спосіб глюкоза вступає на шлях гліколізу. Яка частина уведеної в середовище глюкози піддається розпаду по тому або іншому з названих шляхів, вдається легко визначити, застосовуючи мічені радіоактивні з'єднання. Замічено, що в Aspergіllus nіger, у культурах якого відбувається інтенсивне спороутворення, переважає гліколітичний шлях, у той час як у молодого неспороутворюючого - пентозофосфатний. В іншої культури - Aspergіllus nіdulans - було виявлено значне підвищення функціональної активності пентозофосфатного шляху в період експонентної фази росту, тобто тоді, коли потреба у відновлених коферментах НАДФ для цілей біосинтезу дуже велика. Для з'ясування питання про те, яка частка глюкози асимілюється по гексозомонофосфатному шляху, яка по гліколітичному, використовують методи із застосуванням ізотопної мітки. Одну частину проби інкубують з 14C-1-глюкозою, іншу - з 14С-6-глюкозою. Потім відзначають момент появи мітки в молекулах СО2, що утворюються в результаті окислювання обох субстратів. Якщо в клітинах окислювання глюкози йде по гліколітичному шляху, а потім через цикл трикарбонових кислот, то мітка повинна з'являтися в молекулах СО2 в обох варіантах одночасно. Якщо асиміляція відбувається через гексозомонофосфатний шлях, то мітка буде з'являтися в СО2 спочатку тільки в першому варіанті, тобто з 14С-1-глюкозою.
6.3. Метаболізм вуглеводів, відмінних від глюкози
Як було сказано вище, з'єднання, відмінні від глюкози, наприклад уронові кислоти або багатоатомні спирти, щоб включитися в метаболізм, повинні перетерпіти ряд ензиматичних перетворень. Так, при введенні D-манітола (маніта) у середовище є дві можливості його включення в гліколіз: 1) завдяки активності манітолкінази з утворенням манітол-1-фосфата й далі НАД залежна манітол-1-фосфатдегідрогеназа перетворює його в D-фруктозо-6-фосфат; 2) альтернативний шлях забезпечує одна з манітолдегідрогеназ. Тут утворюється фруктоза, що фосфорилюється до D-фруктозо-6-фосфата. Остання легко перетворюється в D-глюкозо-6-фосфат при участі глюкозо-фосфатізомерази. У такий спосіб маніт вступає на шлях гліколізу. Очевидно, що частина його може включитися в обмін по пентозофосфатному шляху. Іншим прикладом може послужити D-галактуронова кислота, найпростішого представника пектинових речовин. У результаті ряду послідовних реакцій відбувається її ензиматичне перетворення до фосфогліцеринового альдегіду й піровиноградної кислоти:
Манітолдегідрогеназа (КФ 1.1.1.67) має в якості коферменту НАД+, манітолдегідрогеназа (КФ 1.1.1.138) – НАДФ+. До складу середовища іноді вводять лактозу у вигляді чистого або технічного продукту, або лактоза входить у сировину, застосовувана в якості одного з компонентів середовищ, наприклад у молочну сироватку. Лактоза спочатку розщеплюється β-галактозидазою на галактозу й глюкозу, Для асиміляції галактози запропоновані шлях: 1) галактоза+АТФ↔галактозо-1-фосфат+АДФ; 2) D-глюкозо-1-фосфат+УТФ↔УДФ-глюкоза+ФФн; 3) галактозо-1-фосфат +УДФ-глюкоза↔глюкозо-1-фосфат + УДФ-галактоза; 4)УДФ-галактоза↔УДФ-глюкоза. Інший моносахарид, що входить до складу лактози - глюкоза бере участь у цих реакціях у вигляді свого фосфорильованного похідного- глюкозо-1-фосфата; 2) галактоза +АТФ↔галактозо-1-фосфат+АДФ; галактозо-1-фосфат+УТФ↔УДФ-галактсза + ФФн; УДФ-галактоза↔УДФ-глюкоза; УДФ-глюкоза+ ФФН↔глюкозо-6-фосфат+ УТФ. У результаті катаболічних процесів перетворення глюкози утворюється один з важливих продуктів обміну речовин - піровиноградна кислота. Остання є субстратом численних реакцій, особливо при зброджуванні Формально піровиноградна кислота не входить у цикл трикарбонових кислот, однак у результаті серії реакцій піруватдегідрогеназного комплексу утвориться ацетилкофермент.
6.4 Цикл трикарбонових кислот
Цикл трикарбонових кислот, здійснюваний на останньому етапі катаболізму глюкози, одночасно служить для клітини джерелом вихідних продуктів для реакцій біосинтезу. Тут практично сходяться всі шляхи катаболізму. Загальна схема циклу й назви ферментів, що здійснюють процес, представлені на рис. 3.4. Основна функція циклу полягає в дегідруванні оцтової кислоти, що в підсумку приводить до утворення двох молекул CO2 і чотирьох пар атомів водню В циклі відбувається також утворення НАД-Н й АТФ, що йдуть на енергетичні потреби. Як думають, більшість реакцій циклу оборотні, проте, основним напрямком плину ензиматичних реакцій у циклі можна вважати шлях убік утворення щавле-вооцтової кислоти через α-кетоглутарову, бурштинову, фумарову кислоти. Це положення треба через відсутність доказу функціонування α-кетоглутарат-дегідрогеназного комплексу в напрямку синтезу α-кетоглутарової кислоти із сукцината й CO2. Думають, що реакцією, яка лімітує швидкість обороту циклу, є окислювання ізолимонної кислоти до α-кетоглутарової, яке каталізується алостеричним ферментом ізоцитратдегідрогеназою. Для еукаріотів характерна локалізація ферментної системи циклу в мітохондріях, у прокаріотів, що не мають мітохондрій, - у цитоплазматичній мембрані. Мітохондріальна мембрана має здатність до виборчої проникності метаболітів циклу. Так, інтактні (неушкоджені, незруйновані) мітохондрії не пропускають НАД у відновленій формі. Непроникна мітохондріальна мембрана для ацетил-КоА. Останній факт, природно, викликає питання про те, що ж є джерелом ацетил-КоА, який йде на синтез. Продуктом циклу, що легко переходить у цитоплазму крізь мембрану, є лимонна кислота. Вона ж служить вихідним продуктом позамітохондріаль-ного синтезу ацетил-КоА: цитрат+АТФ+HSKoА↔ ацетил-КоА+ оксалоацетат+АДФ+Фн. Друга реакція проходить за участю ацетаттіокінази: ацетат+АТФ+НSКоА↔ацетил-КоА+АМФ+ФФн.
Рисунок 6.4 - Цикл трикарбонових кислот. Гліоксалатний цикл показаний пунктирними лініями. 1- цитратсинтаза, 2 і 3 – аконітаза, 4 і 5 – ізоцитратдегідрогеназа, 6 - α-кетоглутаратдегідрогеназа, 7 – сукцинаттіокіназа, 8 – сукцинатдегідрогеназа, 9 – фумараза, 10 – малатдегідрогеназа, 11 – ізоцитратліаза, 12 - малатсинтаза Високі концентрацій вуглеводів, що присутні у середовищі, можуть придушувати окисні процеси, викликати підвищену активність ферментів гліколізу, і далі посилення процесів бродіння. У зв'язку із цим, якщо шлях біосинтезу цільового продукту пов'язаний з функціонуванням циклу Кребса, необхідно збалансувати вихідну концентрацію вуглеводів і фосфатів у середовищі. Як правило, із циклу Кребса на потреби біосинтезу йде значна кількість проміжних метаболітів (наприклад, на синтез глютамінової кислоти з α-кетоглутарової: ацетил-КоА + щавлевооцтова кислота→лимонна кислота → α-кетоглутарова кислота → глютамінова кислота). У результаті такого процесу із циклу буде йти щавлевооцтова кислота, і цикл перестане функціонувати. Однак цього не відбувається, оскільки існують спеціальні ферментативні механізми, що поповнюють фонд проміжних продуктів циклу. Такі реакції називають анаплеротичними. Одна з таких анаплеротичних реакцій - карбоксилювання пірувата з утворенням щавлевооцтової кислоти:
Очевидно, її концентрація повинна завжди підтримуватися на досить високому рівні, необхідному для ефективного функціонування циклу. Вона необхідна як акцептор ацетил-КоА.
6.5 Гліоксилатний шлях
Анаплеротичну функцію виконує діючий одночасно з циклом Кребса гліоксилатний шунт (цикл). На відміну від першого, де відбувається окислювання оцтової кислоти, в гліоксилатному циклі оцтова кислота йде на синтез. Для функціонування цього циклу необхідно мати два ферменти: ізоцитрат-ліазу, що розщеплює ізолимонну кислоту на бурштинову й гліо-ксилову, і малатсинтазу, яка каталізує приєднання гліоксилової кислоти до ацетил-КоА з утворенням яблучної кислоти (див. рис. 3.4) При кожному обороті гліоксилатного циклу дві молекули ацетил-КоА включаються в цикл. Сумарний результат реакцій, показаних на схемі, полягає в перетворенні цих двох молекул ацетату в молекулу щавлевооцтової кислоти. Одночасно утворюється одна молекула бурштинової кислоти. Ця кислота йде на біосинтез, одна пара атомів водню переноситься від яблучної кислоти до кисню через дихальний ланцюг, регулятором чого є окисне фосфорилювання АДФ. Таким чином, гліоксилатний цикл поставляє для різних процесів біосинтезу як енергію, так і чотирьохвуглецеві проміжні продукти. Особливого значення набуває цикл Кребса в тих випадках, коли ріст мікроорганізмів відбувається на ацетаті чи на субстратах, які ведуть до утворення ацетату, наприклад жирних кислотах, n-алканах. Тут ацетат, утворюючи свою метаболічно активну форму КоА похідної, безпосередньо включається в обмін речовин.
6.6 Регуляція активності ферментів циклу трикарбонових кислот
Значення циклу трикарбонових кислот (ЦТК) як центрального інтегруючого механізму клітинного обміну і його роль у механізмах біосинтезу вимагають звернути особливу увагу на біохімічні механізми регуляції активності ферментів циклу. Ці механізми охоплюють не тільки властиво реакції циклу, але й широке коло суміжних ланок обміну, таких, як дихальний ланцюг і система спряження енергії, біосинтетичні реакції. Складність проблеми збільшується тим, що регуляція здійснюється при участі механізмів, що впливають як на активність ферментів так і на процеси їхнього біосинтезу, тобто на генний рівень. Першою реакцією, яка вводить із цикл ацетил-КоА є окисне декарбоксилювання пірувата, яке каталізується піруватдегідрогеназним комплексом. Регуляція його активності має істотне значення, тому що визначає напрямок обміну пірувата. Ферментний комплекс може активуватися деякими метаболітами, що входять у гліколіз може конкурентно пригнічуватися своїми власними продуктами - НАДН+ й ацетил-КоА. Так, збільшення відношення НАДН/НАД+ від l до 3 викликає 90% зниження швидкості реакції, а збільшення відношення (ацетил-КоА)/КоА приводить до такого ж ефекту. Коли відбувається окислювання жирних кислот, піруватдегідрогеназа помітно інгибується. Напевно, це явище порозумівається супутніми процесу окислювання високими концентраціями АТФ, ацетил-КоА й НАДН. Піруват являється субстратом не тільки для піруватдекарбоксилазного комплексу, але й іншої важливої реакції, яка компенсує витрати в ЦТК, -піруваткарбоксилазна реакція, що поставляє в цикл щавлевооцтову кислоту при карбоксилюванні піровиноградної кислоти за участю АТФ. Першою реакцією ЦТК, є конденсація ацетил-КоА із щавлевооцтовою кислотою, яка каталізується цитратсинтазою. Саме активність цитрасинтази є головною ланкою, яка визначає швидкість потоку в циклі. Стосовно до дріжджів (і, імовірно, більшості еукаріотів) швидкость цитратсинтазної реакції залежить насамперед від концентрації щавлевооцтової кислоти і ацетил-КоА в мітохондріях. Утворення щавлевооцтової кислоти з яблучної є термодинамічно невигідною реакцією. Цитрасинтазна реакція представляє совою досить важливу ланку регуляції не тільки в ЦТК, але й у зв'язаних реакціях, що відіграють першоступеневу роль у інтеграції клітинного обміну. Із цитратом зв'язані початкові етапи синтезу жирів, тому, що цитрат є формою, у вигляді якої ацетил-КоА, утворений у мітохондріях, транспортується через мітохондріальну мембрану й надходить у цитоплазму. У цитоплазмі він знову перетворюється в ацетил-КоА при участі АТФ-залежної цитратліази. Цитрат у дріжджових клітках грає важливу роль у прояві пастерівського ефекту, т е. у гальмуванні бродильної активності подихом, будучи алостеричним інгібітором фосфофруктокінази. Синтез цитрату - стадія, що лімітує швидкість циклу лимонної кисло-ти. Інгібуючий ефект на цитратсинтазу вчиняють НАДН і сукциніл-КоА. Але основний вплив на швидкість синтезу цитрату вчиняє надходження субстрату. Цитрат, що утворився в результаті цитратсинтазної реакції піддається подальшим перетворенням за участю аконітази, яка каталізує оборотні взаємоперетворення цитрату, цис-аконітату й ізоцитрату. Контрольні питання: 1. Розкрити роль вуглеводного обміну в життєдіяльності мікроорганізмів 2.Навести приклад компонентів поживних середовищ – джерел вуглецю 3. Охарактеризувати гліколіз як біохімічний шлях засвоєння вуглеводів 4. Охарактеризувати гексозомонофосфатний цикл як біохімічний шлях засвоєння вуглеводів 5. Охарактеризувати біохімічний шлях засвоєння вуглеводів відмінних від глюкози 6. Охарактеризувати цикл Кребса як біохімічний шлях засвоєння вуглеводів. Регуляція активності ферментів циклу 7. Охарактеризувати гліоксилатний цикл як біохімічний шлях засвоєння вуглеводів
Поиск по сайту: |